
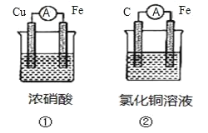
【题目】(1)为了验证 Fe2+与 Cu2+氧化性强弱,下列装置能达到实验目的的是_______(填装置序号), 其正极的电极反应式为_______;若构建该原电池时两个电极的质量相等,当导线中通过 0.4 mol 电子时,两个电极的质量差为_______g。
(2)将 CH4 设计成燃料电池,其利用率更高,装置如图所示(A、B 为多孔碳棒)。

实验测得 OH- 定向移向 A 电极,则_______(填 A 或 B)处电极入口通 CH4,其电极反应式为_______。
(3)金属冶炼和处理常涉及氧化还原反应。由下列物质冶炼相应金属时采用电解法的是_______(填选 项字母)。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
【答案】② Cu2++2e-=Cu 24 A CH4-8e-+10OH-=CO32-+7H2O b d
【解析】
(1)验证 Fe2+与 Cu2+氧化性强弱,发生反应Fe+Cu2+==Fe2++Cu, 由此反应确定所用装置及正极的电极反应。当导线中通过 0.4 mol 电子时,负极Fe失电子生成Fe2+,质量减轻,正极Cu2+得电子生成Cu,质量增加,两个电极的质量差为两电极质量变化之和。
(2)OH-带负电性,应向负极移动,由此确定A 电极为负极,CH4在碱性溶液中失电子生成CO32-等。
(3)金属冶炼和处理时,由于钾、钙、钠、镁、铝活泼,难以用还原剂还原,所以常使用电解法。
(1)A装置中Cu作负极,发生反应Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O,没有涉及Fe,不能验证 Fe2+与 Cu2+氧化性强弱;要发生反应Fe+Cu2+==Fe2++Cu, 应使用装置②,正极的电极反应为Cu2++2e-=Cu。在电池②中,有如下关系式:Fe—2e—Cu,则参加反应的Fe与生成的Cu都为0.2mol,两个电极的质量差为0.2mol ×64g/mol+0.2mol ×56g/mol=24g。答案为:②;Cu2++2e-=Cu;24;
(2)在原电池中,阳离子向正极移动,阴离子向负极移动,因为OH-向A电极移动,所以A 电极为负极,CH4在KOH溶液中失电子生成CO32-、H2O,电极反应式为CH4-8e-+10OH-=CO32-+7H2O。答案为:A;CH4-8e-+10OH-=CO32-+7H2O;
(3) a.用Fe2O3冶炼Fe,需使用还原剂(常为CO),用还原法炼铁,a不合题意;
b.用NaCl冶炼Na,一般的还原剂不能满足要求,应使用电解法,b符合题意;
c.用Cu2S冶炼Cu,需使用氧化剂(纯氧),用氧化法将Cu2S氧化为Cu,c不合题意;
d.用Al2O3冶炼Al,一般氧化剂不能满足要求,需使用电解法,d符合题意;
故选bd。答案为:bd。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有__________个原子共面;
(2)金刚烷的分子式为____________________,其分子中的CH2基团有__________个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
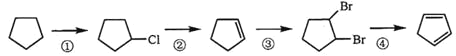
其中,反应①的产物名称是_____________,反应②的反应试剂和反应条件是_________,反应③的反应类型是_____________;
(4)已知烯烃能发生如下的反应:  ,请写出下列反应产物的结构简式:
,请写出下列反应产物的结构简式: ___________。
___________。
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基],写出A的一种结构简式(不考虑立体异构):________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )

A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是难溶氢氧化物在不同pH下的溶解度(S),下列说法正确的是( )
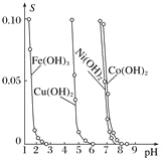
A. pH=3时溶液中铁元素的主要存在形式是Fe3+
B. 若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法除去
C. 若要分离溶液中的Fe3+和Cu2+,可调节溶液的pH为4
D. 若向含有相同物质的量浓度的Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KI溶液在酸性条件下能与氧气反应。现有以下实验记录:
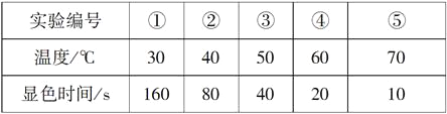
回答下列问题:
(1)该反应的离子方程式为_____________________________________。
(2)该实验的目的是__________________________________。
(3)实验试剂除了1 mol·L-1KI溶液、0.1 mol·L-1H2SO4溶液外,还需要的试剂是________,实验现象为_____________________________。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是________(填字母)。
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是_________________________。
(6)若要进行溶液酸性大小对反应速率的影响的探究实验,你会采取的措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)[化学——选修5:有机化学基础]
近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下:

已知:![]()
回答下列问题:
(1)A的化学名称是________________。
(2)B为单氯代烃,由B生成C的化学方程式为________________。
(3)由A生成B、G生成H的反应类型分别是________________、________________。
(4)D的结构简式为________________。
(5)Y中含氧官能团的名称为________________。
(6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。
(7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸是重要的有机合成原料及合成树脂单体,可通过以下方式制得:CH![]() CH
CH![]() CH2=CHCOOH,下列有关说法错误的是( )
CH2=CHCOOH,下列有关说法错误的是( )
A. CO分子的碳氧叁键中存在配位键
B. 丙烯酸分子中σ键与π键的个数比为4∶1
C. 乙炔和水均为极性分子
D. 丙烯酸具有酸性,且能发生加成反应、聚合反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定溶液中一定能大量共存的离子组是
A. 含有大量AlO![]() 的溶液中:Na+、K+、HCO3-、NO3-
的溶液中:Na+、K+、HCO3-、NO3-
B. pH=1的溶液中:NH4+、Na+、Fe3+、SO42-
C. 水电离产生c(H+)=1×10-13 mol/L溶液中:K+、Al3+、Cl-、SO42-
D. Na2S溶液中:SO42-、K+、Cu2+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com