
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )

A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
科目:高中化学 来源: 题型:
【题目】表中的W、X、Y、Z均为短周期元素,其原子最外层电子数之和为22。下列说法不正确的是( )
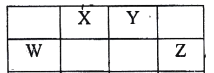
A.以上元素都可以与H元素形成18电子的分子
B.X的氧化物都不是酸性氧化物
C.Y与金属钠形成的化合物可能含有非极性共价键
D.1mol W的单质与足量的Z的单质反应,转移电子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下如图所示,是原电池的装置图。请回答:
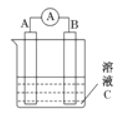
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe,A极材料为铜,A为______极,A电极上发生的电极反应式为___________________________,反应进行一段时间后溶液C的c(H+)将___________(填“变大”“减小”或“基本不变”)。
(2)若C为CuSO4溶液,B电极材料为Zn,A极材料为铜。则B为_________极,B极发生________反应(填“氧化或还原),B电极上发生的电极反应为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置进行相应实验,能达到实验目的的是( )
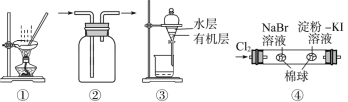
A. 用图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 按装置②所示的气流方向可用于收集H2、NH3等
C. 用图③所示装置,分离CCl4萃取I2水后的有机层和水层
D. 用图④所示装置,可以证明氧化性:Cl2>Br2>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天宫二号空间实脸室己于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________,该物质的属于_______ 氧化物 ,实验室中不能用玻璃塞试剂瓶盛KOH溶液,原因是_________________________________(用离子方程式表示)。
(2)联氨(N2H4,无色液体)可用作火箭燃料,其电子式为____________。
(3)太阳能电池帆板是“天宫二号”空间运行的动力湃泉。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光认太阳能电池,该电池的核心材料是___________,其能量转化方式为____________________。
(4)下面是一个还原过程的反应式:NO3﹣+4H++3e﹣→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生.
①写出并配平该氧化还原反应的方程式:_________________________________
②反应中若产生0.2mol气体,则转移电子的物质的量是___mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,正确的是( )
A.铁与硝酸反应时,其他条件一定时,硝酸越浓,反应速率越快
B.在金属钠与足量水反应中,增加水的量能加快反应速率
C.在2SO2+O2![]() 2SO3反应中加入18O2,达到平衡后SO2中不可能含有18O2
2SO3反应中加入18O2,达到平衡后SO2中不可能含有18O2
D.无论是吸热还是放热反应,加热都能加快化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组探究甲烷与氯气的取代反应,装置、现象如下:
现象 |
ⅰ.光照后,产生白雾,混合气体颜色变浅 ⅱ.试管内液面上升至试管的2/3;试管壁和液面上出现少量油状液滴 |

下列说法不正确的是
A. 饱和食盐水可以减少氯气的溶解
B. 油状液滴的主要成分是一氯甲烷
C. 产生白雾以及试管内液面上升证明有氯化氢生成
D. 为了探究反应条件,可用黑色纸套套住装满甲烷和氯气的试管,一段时间后进行观察
查看答案和解析>>
科目:高中化学 来源: 题型:
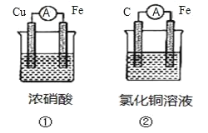
【题目】(1)为了验证 Fe2+与 Cu2+氧化性强弱,下列装置能达到实验目的的是_______(填装置序号), 其正极的电极反应式为_______;若构建该原电池时两个电极的质量相等,当导线中通过 0.4 mol 电子时,两个电极的质量差为_______g。
(2)将 CH4 设计成燃料电池,其利用率更高,装置如图所示(A、B 为多孔碳棒)。

实验测得 OH- 定向移向 A 电极,则_______(填 A 或 B)处电极入口通 CH4,其电极反应式为_______。
(3)金属冶炼和处理常涉及氧化还原反应。由下列物质冶炼相应金属时采用电解法的是_______(填选 项字母)。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛镍合金被称为记忆合金,是一种具有独特形状记忆功能、耐磨损、抗腐蚀、超弹性等特点的功能材料,主用于航空航天、医疗等领域。回答下列问题:
(1)基态镍原子的价电子排布式为 __________,其所在周期第一电离能最小的元素名称为__。
(2)钛铁矿经过 H2SO4、HNO3等多种物质处理后会生成硫酸氧钛等中间产物。
①硫酸氧钛晶体中阳离子为如图1所示链状聚合形式的离子,该晶体的化学式为_,晶体中存在的微粒间作用力有离子键、___和____。

②查资料知H2SO4和HNO3的沸点分别为338℃和83℃,试分析差异大的主要原因__。
(3)镍是人体必需的微量元素,但超量中毒易过敏或诱发癌症。急性镍中毒通常用二乙基二硫代氨基钠(结构如图2)解毒,该物质中碳原子的杂化方式有___。

(4)Ni、O、Cr 可以形成一种具有特殊导电性的复合氧化物晶胞结构如图3。若晶胞参数为apm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为__pm。设阿伏加德罗常数数值为NA,则该晶体密度为__g·cm-3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com