
【题目】如图所示是制取溴苯的装置。回答下列问题:
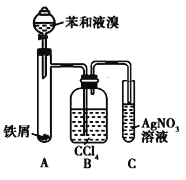
(1)装置C中观察到的现象是_____,证明_____。
(2)装置B是吸收瓶,瓶内盛有CCl4,实验中观察到的现象是_____,原因是_____;
(3)如果没有装置B,将装置A、C直接相连,则该套实验装置 _____(填“合理”或 “不合理”),原因是_____。
(4)实验完毕后,将装置A试管中的液体倒入盛有冷水的烧杯中,烧杯_____(填“下”或“上”)层为溴苯。
【答案】导管口有白雾出现,试管中有浅黄色沉淀产生 有HBr生成 B中导气管口有气泡生成,CCl4颜色由无色逐渐变为橙红色 装置A中的溴化氢、溴蒸气和苯蒸气通过导管进入到装置B中,所以导管口有气泡;装置A中的溴蒸气逸出并溶于CCl4中,所以CCl4颜色由无色逐渐变为橙红色 不合理 溴蒸气也能和AgNO3反应生成AgBr 下
【解析】
实验制备溴苯的反应原理为:2Fe+3Br2=2FeBr3,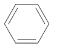 +Br2
+Br2![]()
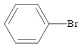 +HBr。图中,装置A为
+HBr。图中,装置A为 和Br2在FeBr3的催化下发生反应,由于反应放热,苯和液溴易挥发导致所得溴苯不纯净,装置B中CCl4的作用是除去HBr气体中的苯蒸气和溴蒸气。装置C中加入了AgNO3溶液,会与HBr发生反应:AgNO3+HBr=AgBr↓+HNO3,生成浅黄色沉淀。据此进行分析。
和Br2在FeBr3的催化下发生反应,由于反应放热,苯和液溴易挥发导致所得溴苯不纯净,装置B中CCl4的作用是除去HBr气体中的苯蒸气和溴蒸气。装置C中加入了AgNO3溶液,会与HBr发生反应:AgNO3+HBr=AgBr↓+HNO3,生成浅黄色沉淀。据此进行分析。
(1)装置C中为HBr与AgNO3反应生成AgBr,故观察到的现象是导管口有白雾出现,试管中有浅黄色沉淀产生,证明了有HBr生成。答案为:导管口有白雾出现,试管中有浅黄色沉淀产生;有HBr生成;
(2)装置A中的溴化氢、溴蒸气和苯蒸气通过导管进入到装置B中,可以看到B中导气管口有气泡生成,根据相似相溶原理,溴易溶于CCl4中,故而CCl4因为溶解了溴蒸气,其颜色由无色逐渐变为橙红色。答案为:B中导气管口有气泡生成,CCl4颜色由无色逐渐变为橙红色;装置A中的溴化氢、溴蒸气和苯蒸气通过导管进入到装置B中,所以导管口有气泡;装置A中的溴蒸气逸出并溶于CCl4中,所以CCl4颜色由无色逐渐变为橙红色;
(3)因为溴蒸气也能和AgNO3反应生成AgBr,故若是没有装置B,将装置A、C直接相连,则该套实验装置设置不合理,答案为:不合理;溴蒸气也能和AgNO3反应生成AgBr;
(4)溴苯的密度大于水的密度,且不溶于水,故将装置A试管中的液体倒入盛有冷水的烧杯中,烧杯下层为溴苯,答案为:下。


科目:高中化学 来源: 题型:
【题目】(10分)根据下列变化关系:

请填空:
(1)A物质的名称_____ 。B溶液为____________.作用为_________________________
(2)写出④、⑥两步反应的化学方程式,在( )号中标明反应类型。
④ ________________________________________( )
⑥_______________________________________________( )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
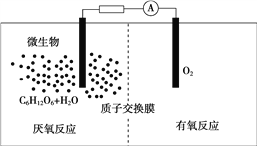
A. 微生物促进了反应中电子的转移
B. 正极反应中有CO2生成
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的分子,下列叙述正确的是( )
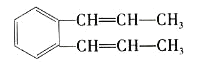
A.该分子最多有22个原子在同一平面内
B.1mol该物质完全燃烧消耗16molO2
C.除苯环外的其余碳原子有可能在一条直线上
D.1mol该物质与足量溴水反应,最多消耗5molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将amol氮气与bmol氢气的混合气体通入一个固定容积的密闭容器中,发生反应N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,则a值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中氨气体积分数为25%,平衡时氨气的物质的量为________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同)n始∶n平=________。
(4)原气体中a∶b=________。
(5)达到平衡时,N2和H2的转化率之比α(N2)∶α(H2)=________。
(6)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氧化钠和过氧化钠的叙述正确的是( )
A. 氧化钠比过氧化钠稳定
B. 都能与二氧化碳、水反应产生氧气
C. 所含氧元素的化合价都为-2价
D. 阴阳离子的个数比都为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于0.1mol/LH2SO4溶液的叙述错误的是
A.1L该溶液中含有H2SO4的质量为9.8g
B.0.5L该溶液中氢离子的物质的量浓度为0.2mol/L
C.从1L该溶液中取出100mL,则取出的溶液中H2SO4的物质的量浓度为0.01mol/L
D.取该溶液10mL加水稀释至100mL后,H2SO4的物质的量浓度为0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个密闭容器中分别充入Ne、H2、O2三种气体,在以下各种情况下排序正确的是( )
A.当它们的体积、温度和压强均相同时,三种气体的密度ρ(H2)>ρ(Ne)>ρ(O2)
B.当它们的温度和密度都相同时,三种气体的压强p(H2)>p(Ne)>p(O2)
C.当它们的质量、温度和压强均相同时,三种气体的体积V(O2)>V(Ne)>V(H2)
D.当它们的压强、体积和温度均相同时,三种气体的质量m(H2)>m(Ne)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。下列说法正确的是( )
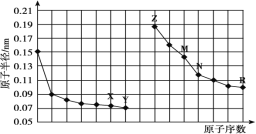
A.最高价氧化物对应水化物的碱性:Z<M
B.Y、R两种元素气态氢化物的稳定性:Y>R
C.X、N两种元素形成的化合物属于离子化合物
D.简单离子的半径:Z>M>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com