
用质量均为100 g的铜作电极,电解硝酸银溶液,电解一段时间后,两电极的质量差为28 g,此时两电极的质量分别为
A.阳极100 g,阴极128 g B.阳极91.0 g,阴极119.0 g
C.阳极93.6 g,阴极121.6 g D.阳极86.0 g,阴极114.0 g
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
有关键能(破坏1 mol共价键吸收的能量)数据如表
化学键 | Si—O | O===O | Si—Si |
键能/kJ·mol-1 | X | 498.8 | 176 |
晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)===SiO2(s) ΔH=-989.2 kJ·mol-1,则X的值为(已知1 mol Si中含有2 mol Si—Si键,1 mol SiO2中含有4 mol Si—O键)
A.423.3 B.460 C.832 D.920
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二第一学期化学试卷(解析版) 题型:填空题
(14分)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子最外层电子排布为3s23p1,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)则W为 ,X为 ,Y为 ,Z为 。(填元素符号)
W的气态氢化物稳定性比H2O(g) (填“强”或“弱”)。
(2)Z原子的基态原子核外电子排布式是 ,Y的电负性比X的________(填“大”或“小”),W的第一电离能比O的 (填“大”或“小”)。
(3)X的最高价氧化物对应水化物与NaOH溶液反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:填空题
(14分)Cl2是一种重要的化工原料。
(1)电解饱和NaCl溶液获得Cl2的化学方程式是____________________。
(2)为便于储存,要将氯气液化[ Cl2(g)  Cl2(l) ],应采取的措施是_____(写出一条即可)。
Cl2(l) ],应采取的措施是_____(写出一条即可)。
(3)液氯储存区贴有的说明卡如下(部分):
危险性 |
|
储运要求 | 远离金属粉末、氨、烃类、醇更物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
包装 | 钢瓶 |
① 用离子方程式表示“泄漏处理”中NaHSO3溶液的作用_______。
② 若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③ 氯气含量检测仪工作原理示意图如下图甲所示,则Cl2在Pt电极放电的电极反应式是_______。

(4)质量标准要求液氯含水量(以1 g氯气含水的质量计)<0. 4 mg,含水量超标会严重腐蚀钢瓶。液氯含水量的测定装置如上图乙所示:
① 用离子方程式说明c装置的作用_______。
② 检测液氯的含水量,根据上图,需要测定的数据是_______。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系的比较正确的是
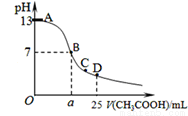
A.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.在C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
在一定条件下,发生CO(g)+NO2(g) CO2(g)+NO(g)ΔH <0的反应,达到平衡后,保持体积不变,降低温度,混合气体的颜色
CO2(g)+NO(g)ΔH <0的反应,达到平衡后,保持体积不变,降低温度,混合气体的颜色
A.变深 B.变浅 C.不变 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:填空题
(每空2分,共16分)
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:
N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)该反应的平衡常数表达式为:K=
(2)若反应进行到某时刻t时,nt(N2)=8 mol,nt(NH3)=4 mol,计算 a= 。当反应达到平衡时,混合气体的体积为537.6 L(标况下),其中NH3的含量(体积分数)为25%。原混合气体中, a:b= 。
Ⅱ、反应mA+nB pC+qD在某温度下达到平衡。
pC+qD在某温度下达到平衡。
①若A、B、C 、D都是气体,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时C的物质的量浓度变为原来的1.6倍,则m、n、p、q的关系是m+n p+q(填“<”或“>”或“=”) 。
②若A、B、C ,D都为气体,且m+ n = p+q,则将气体体积压缩后A的物质的量将 _________(填“减小”“增大”“不变”),平衡______移动。(填“正向”或“逆向”或“不”)
③若给体系升温,B的物质的量减少,则正反应为 ________反应(填“放热”或“吸热”)
④若在体系中增加A的量,平衡不发生移动,则A肯定不能为_____态。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:选择题
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是
A.锌作阳极,镀件作阴极,溶液中含有锌离子
B.铂作阴极,镀件作阳极,溶液中含有锌离子
C.铁作阳极,镀件作阴极,溶液中含有亚铁离子
D.锌用阴极,镀件作阳极,溶液中含有锌离子
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:填空题
(6分)现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物。某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应)。

请回答:
 (1)气体W的化学式是 。
(1)气体W的化学式是 。
(2) 溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有 。
溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有 。
(3)反应②和③之后均需进行的操作的名称是 。
(4)试剂Y是 (填化学式)。
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com