
����Ŀ����50mL NaOH��Һ����������ͨ��һ������CO2�����ȡ����Һ10mL����ϡ�͵�100mL�������ϡ�ͺ����Һ����μ���0.1mol/L��HCl��Һ��������CO2�������(��״����)���������HCl�����֮��Ĺ�ϵ��ͼ��ʾ��
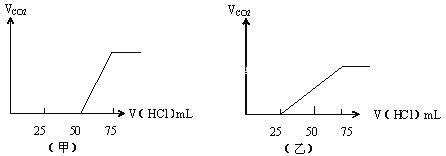
��
(1)NaOH������CO2������ڼס�����������£�������Һ�д��ڵ������Ǽף�________�������ʵ���֮���ǣ�________���ң�__________�������ʵ���֮���ǣ�__________��
(2)������������²�����CO2����(��״��)���Ǽף�________mL���ң�_________mL��
(3)ԭNaOH��Һ�����ʵ���Ũ����_________������Na2O2��������ˮ���100mL��Һ�����Na2O2_______g��
���𰸡�NaOH��Na2CO3 1:1 NaHCO3��Na2CO3 1:1 56mL 112mL 0.75mol/L 2.9g
��������
��Ӧ�����Һ�еμ����ᣬ����ʼ����CO2����ʱ��������ӦNaHCO3+HCl=NaCl+H2O+CO2����
(1)(��)�п�ʼ����CO2�������������HClΪ25mL��֮ǰ����50mL���ᣬ��������̼��NaOH��Ӧ����Һ�в���NaHCO3����Na2CO3+HCl=NaHCO3+NaCl��֪����CO32-ת��ΪHCO3-Ӧ����HClΪ25mL��˵���ýλ�������ӦNaOH+HCl=NaCl+H2O����Һ������ΪNaOH��Na2CO3���ݴ˼���NaOH��Na2CO3�����ʵ���֮�ȣ�
(��)�п�ʼ����CO2�������������HClΪ50mL��֮ǰ����25mL���ᣬ��������̼��NaOH��Ӧ����Һ�в���NaHCO3����Na2CO3+HCl=NaHCO3+NaCl��֪����CO32-ת��ΪHCO3-Ӧ����HClΪ50mL��˵���ý�ֻ����Na2CO3+HCl=NaHCO3+NaCl���Ҷ�����̼��NaOH��Ӧ����Һ�к�NaHCO3��Na2CO3�����ݷ�Ӧ����������������NaHCO3��Na2CO3�����ʵ���֮�ȣ�
(2)����̼Ԫ���غ㣬���NaHCO3+HCl=NaCl+H2O+CO2���������ɵĶ�����̼�������
(3)����75mL����ʱ����Һ������ֻ��NaCl������Ԫ���غ����ԭ����������Һ��Ũ�Ⱥ���Ҫ�Ĺ������Ƶ�������
��Ӧ�����Һ�еμ����ᣬ����ʼ����CO2����ʱ�������ķ�ӦΪNaHCO3+HCl=NaCl+H2O+CO2����
(1)����(��)ͼ����ʼ����CO2���������Ĺ���������HClΪ25mL����������̼��NaOH��Ӧ����Һ�в���NaHCO3����Na2CO3+HCl=NaHCO3+NaCl��֪����CO32-ת��ΪHCO3-Ӧ����HClΪ25mL����ͼ���п�ʼ����CO2����ʱ����HCl���Ϊ50mL��˵���ýλ�������ӦNaOH+HCl=NaCl+H2O����Һ������ΪNaOH��Na2CO3���к�NaOH����HCl�����Ϊ50mL-25mL=25mL���ɷ���ʽ��֪NaHCO3��Na2CO3�����ʵ���֮�ȵ����������̷ֱ�������������֮�ȣ���NaOH��Na2CO3�����ʵ���֮��=25mL��25mL=1��1��
(��)�п�ʼ����CO2�������������HClΪ50mL����������̼��NaOH��Ӧ����Һ�в���NaHCO3����Na2CO3+HCl=NaHCO3+NaCl��֪����CO32-ת��ΪHCO3-Ӧ����HClΪ50mL����ͼ���п�ʼ����CO2����ʱ����HCl���Ϊ25mL��˵���ý�ֻ����Na2CO3+HCl=NaHCO3+NaCl���Ҷ�����̼��NaOH��Ӧ����Һ�к�NaHCO3��Na2CO3��Na2CO3ת��ΪNaHCO3�����������Ϊ25mL����ԭ��Һ��NaHCO3�����������50mL-25mL=25mol����NaHCO3��Na2CO3�����ʵ���֮��=25mL��25mL=1��1���ʴ�Ϊ��NaOH��Na2CO3��1��1��NaHCO3��Na2CO3��1��1��
(2)����̼Ԫ���غ㣬(��)�д�50mL��75mL����25mL����ʱ���ɶ�����̼���ý����ɵĶ�����̼Ϊ0.025L��0.1mol/L=0.0025mol�����Ϊ0.0025mol��22.4L/mol=0.056L=56mL����(��)�д�25mL��75mL����50mL����ʱ���ɶ�����̼���ý����ɵĶ�����̼Ϊ0.05L��0.1mol/L=0.005mol�����Ϊ0.005mol��22.4L/mol=0.112L=112mL���ʴ�Ϊ��56��112��
(3)����75mL����ʱ����Һ�����ʶ�ǡ����ȫ��Ӧ����ʱ��Һ��ֻ����NaCl������Ԫ���غ��֪��n(NaOH)=n(NaCl)=n(HCl)=0.075L��0.1mol/L=0.0075mol����ԭ����������Һ��Ũ��=![]() =0.75mol/L������Na2O2��������ˮ���100mL����Һ�������������غ�n(Na2O2)=
=0.75mol/L������Na2O2��������ˮ���100mL����Һ�������������غ�n(Na2O2)=![]() =0.0375mol����m(Na2O2)=0.0375mol��78g/mol=2.925g����Ҫ����2.9g Na2O2���ʴ�Ϊ��0.75mol/L��2.9��
=0.0375mol����m(Na2O2)=0.0375mol��78g/mol=2.925g����Ҫ����2.9g Na2O2���ʴ�Ϊ��0.75mol/L��2.9��


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. CaCO3(s)===CaO(s)��CO2(g)�����²����Է����У�˵���÷�Ӧ�Ħ�H<0
B. ��ͭ����Ʒ�Ʋ����������Ʒ������ǰ����������
C. N2(g)��3H2(g) ![]() 2NH3(g)����H<0��������������ʱ�����¶ȣ���Ӧ����v(H2)��H2��ƽ��ת���ʾ�����
2NH3(g)����H<0��������������ʱ�����¶ȣ���Ӧ����v(H2)��H2��ƽ��ת���ʾ�����
D. ˮ�����ӻ�����KW�����¶ȵ����߶�����˵��ˮ�ĵ����Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na��Mg��Al��Fe���ֽ�����������ɵĻ����12g�����������ᷴӦ�ų�H2 0.5 g����״�������������бض����еĽ�����
A.��B.þC.��D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W һ�ֺ��ص�������Ϊ 18��������Ϊ 10��X �� Ne �ĺ�����������1����Z���ڵ������У�ZԪ�ص�ԭ�ӵõ���������ǿ������Ԫ�ص�����������֮��Ϊ18�� ��ش��������⣺
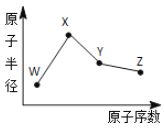
(1)XԪ��λ��Ԫ�����ڱ���λ��Ϊ_____________��
(2)X�ĵ��ʺ� Y �ĵ�����ȣ��۵�ϸߵ���____________(д��ѧʽ) ��Z������ļ��⻯���У��е���ߵ���________(д��ѧʽ)��ԭ��Ϊ______________________��
(3)W��X��Z����Ԫ���γɵĻ������л�ѧ������Ϊ_______��X2W2�ĵ���ʽΪ_______��
(4)Z��������ܶ࣬����һ�ֻ���ɫ���� M����������Ϊ 47.41����������ˮ������ M ��Һ̬��Ũ����̬ʱ���б�ը�� �� M �Ļ�ѧʽΪ___________��M����NaOH��Һ��Ӧ���������ȶ����Σ����ǵ����ʵ���֮��Ϊ 1�U5���÷�Ӧ�Ļ�ѧ����ʽΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ӵļ���˵����ȷ����
A.��ij��Һ�е����������ᣬ��۲쵽��ɫ��ζ���������������ʹ����ʯ��ˮ����ǣ���֤����Һ�бض���![]()
B.��ij��ɫ��Һ�м���BaCl2��Һ���а�ɫ�������֣��ټ���ϡ���ᣬ��������ʧ����֤����Һһ������![]()
C.��ij��ɫ��Һ�м�������ϡ����������Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿڣ�����ֽ����������˵������Һ����![]()
D.������ɫ���ܲ����ܹ��۲쵽��ɫ���棬��һ���м�Ԫ�أ�һ����������Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮú���ǹ�ҵ�ϳɰ���ԭ����������Ҫ�ɷ�ΪH2��CO��CO2��N2��H2O(g)����ˮú���������в���ת��Ϊ�ϳɰ���ԭ�ϡ�
![]()
��1)����I��CO�任��Ӧ�������仯����ͼ��ʾ��

��CO�任��Ӧ���Ȼ�ѧ����ʽ��________________��
��һ�������£�������̶����ܱ������г���aL��ˮú��������CO�任��Ӧ����ò�ͬ�¶ȣ�T1��T2�����������������(H2)��ʱ��Ĺ�ϵ������ʾ��
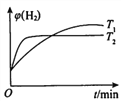
i��T1��T2�Ĵ�С��ϵ���ж�������______________��
ii��������ͼ�л���������������ͬʱ����ʼ����0.5aL��ˮú����T2�¶������������������( H2)��ʱ��ı仯���ߡ�______________
(2)������ñ���Na2CO3��Һ�����ռ��ѳ�CO2ʱ�������������������й���������
����Һ������Ũ�ȹ�ϵ��ȷ����__________��ѡ����ĸ����
a������ǰ��c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)
b�����ճ��ڣ�2c(CO32-)+2 c(HCO3-)+2c(H2CO3)=c(Na+)
c������ȫ���̣�c(Na+)+c( H+)=2c(CO32-)+ c(HCO3-)+ c(OH-)
�ں�����������ijɷּ����������ԭ����___________��
�۵����ռ�ʧЧʱ����д��һ�ֿ�ʹ�������ķ������û�ѧ����ʽ��ʾ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ������ͼ��ʾװ�ý������ĵ绯ѧ��ʴԭ����̽��ʵ�飺
װ�� | �ֱ���еIJ��� | ���� |
| i. ����װ��һ��ʱ������ձ��еμӷ�̪ | |
ii. ����װ��һ��ʱ������ձ��еμ�K3[Fe(CN)6]��Һ | ��Ƭ���������ɫ���� |
(l)С��ͬѧ��Ϊ�������ּ��鷽��������֤���������˵绯ѧ��ʴ��
��ʵ��i�е�������____��
���û�ѧ�������ʵ��i�е�����____��
(2)�������ϣ�K3[Fe(CN)6]���������ԡ�
�پݴ���ͬѧ��Ϊ��ͨ��ii��������֤���������˵绯ѧ��ʴ�������� __________��
�ڽ�������ʵ�飬��ʵ�鼸���Ӻ�ļ�¼���£�
ʵ�� | �ι� | �Թ� | ���� |
| 0.5 mol��L-1 K3[Fe(CN)6]��Һ | iii. ����ˮ | �����Ա仯 |
iv. 1.0 mol��L-1 NaCl ��Һ | ��Ƭ�������������ɫ���� | ||
v. 0.5 mol��L-1 Na2SO4��Һ | �����Ա仯 |
a������ʵ���������____�����£�K3[Fe(CN)6]��Һ��������Ƭ������Ӧ��
b��Ϊ̽��Cl-�Ĵ��ڶԷ�Ӧ��Ӱ�죬С��ͬѧ����Ƭ��ϴ����ϡ������ݺ�ϴ�������ٽ���ʵ��iii��������Ƭ���������ɫ�������˲���ʵ�����Cl-��������____��
(3)��ͬѧ��Ϊ����ʵ���Բ��Ͻ���Ϊ��һ��̽��K3[Fe(CN)6]�������Զ�ʵ��ii�����Ӱ�죬������(2)��װ�ü���ʵ�顣������֤ʵ����Ӱ��ȷʵ���ڵ���____________������ĸ��ţ���
ʵ�� | �Լ� | ���� |
A | ��ϴ�����Ƭ��K3[Fe(CN)6]��Һ���ѳ�O2�� | ������ɫ���� |
B | ��ϴ�����Ƭ��K3[Fe(CN)6]��NaCl�����Һ��δ��O2�� | ������ɫ���� |
C | ��Ƭ��K3[Fe(CN)6]��NaCl�����Һ���ѳ�O2�� | ������ɫ���� |
D | ��Ƭ��K3[Fe(CN)6]����������Һ���ѳ�O2�� | ������ɫ���� |
�ۺ�����ʵ�����������ʵ��ii���Լ���֤ʵ�������˵绯ѧ��ʴ��ʵ�鷽���� _________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���3molA��1molBͶ���ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A��g��+B��g��![]() xC��g��+2D��g����2minĩ��ô�ʱ������C��D��Ũ��Ϊ0.2mol/L��0.4mol/L������������ȷ���� �� ��
xC��g��+2D��g����2minĩ��ô�ʱ������C��D��Ũ��Ϊ0.2mol/L��0.4mol/L������������ȷ���� �� ��
A. x=2
B. 2minʱ��B��Ũ��Ϊ0.4mol/L
C. 0��2min��B�ķ�Ӧ����Ϊ0.2mol��L����min��
D. ��ʱA��ת����Ϊ40��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���·�Ӧ�е���������������Ԫ����ɣ�����a�ķ������幹��Ϊ���������Σ����a���ʵ�����Ԫ�ص�ԭ������֮��С��10�����b���ʵ�Ԫ��Ϊ��������Ԫ�ء������ж���ȷ����
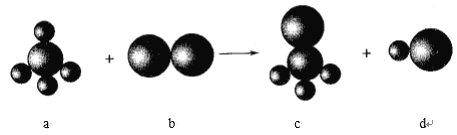
A. ���ַ����еĻ�ѧ�����Ǽ��Լ�
B. a��c����������ԭ�Ӿ�����sp3�ӻ�
C. ���ַ����м�����������������
D. b��d�����й��ۼ��ļ��ܣ�b>d
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com