
【题目】下列有关化学用语表示正确的是( )
A.纯碱的化学式:NaOH
B.氟原子的结构示意图:![]()
C.光导纤维的主要成分:Si
D.明积[KAl(SO4)2·12H2O]溶于水后的电离方程式:KAl(SO4)2=K++Al3++2SO42-
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是( )
A.CH4O,C3H4O5,C2H4O2B.C3H6,C3H8O,C4H8O3
C.C3H8,C4H6,C4H8OD.C2H6,C4H6O,C3H8O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A. 容器内n(A2):n(B2):n(AB)=1:1:2
B. 容器内气体的密度不随时间变化
C. 容器内气体的总压强不随时间变化
D. 单位时间内生成2n mol AB,同时生成n mol A2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车(标志为“![]() ”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
A. 电动汽车的使用有助于减少氮氧化物的排放
B. 燃油汽车也可以悬挂该标志
C. 电动汽车使用时涉及化学能与电能的转换
D. 电动汽车充电、放电过程均有电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学依照如图所示流程提取海带中的碘元素。
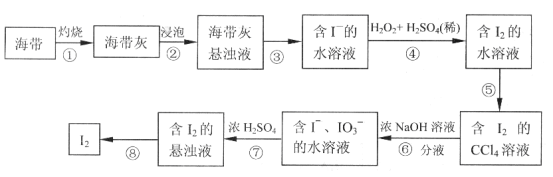
(1)步骤①中灼烧海带所用的仪器是___(填序号)。
a.试管 b.坩埚 c.烧杯 d.锥形瓶
(2)步骤④中用硫酸酸化的H2O2溶液将I-氧化成I2,反应的离子方程式是__。
(3)步骤⑤中采用的分离方法是___。
(4)经步骤⑤得到含I2的CCl4溶液后,继续采取步骤⑥⑦的目的是__。
(5)步骤⑦的反应中,当1molIO3-发生反应时,转移电子的物质的量是__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均速率υ(X)为
A.υ(NH3)═0.04mol·L﹣1·s﹣1B.υ(O2)═0.015mol·L﹣1·s﹣1
C.υ(N2)═0.02mol·L﹣1·s﹣1D.υ(H2O)═0.02mol·L﹣1·s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组查阅资料得知:保险粉(Na2S2O4)和KOH的混合溶液能定量吸收O2:CuCl的盐酸溶液能定量吸收CO,且易被O2氧化。拟设计实验方案,采用上述两种溶液和KOH溶液及量气装置,测定高炉煤气中CO、CO2、N2和O2的百分组成。下列说法不正确的是

A. 采用上述3种吸收剂,气体被逐一吸收的顺序应该是CO2、O2和CO
B. 保险粉(Na2S2O4)和KOH的混合溶液吸收O2的离子方程式为2S2O42-+3O2+4OH-=4SO42-+2H2O
C. 反应结束,恢复至室温,调整水准管内液面与量气管液面齐平,可观察到量气管液面下降
D. 其他两种吸收剂不变,O2的吸收剂可以用灼热的铜网替代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下:
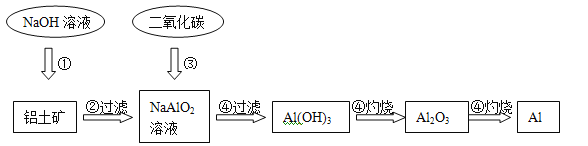
(1)请用离子方程式表示以上工艺流程中第①步反应:__ _______。
(2)写出以上工艺流程中第③步反应的化学方程式:_ _____。
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式_____________。请举一例该反应的用途_____________。
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com