
ЁОЬтФПЁПЪЙЗДгІ4NH3(g)+3O2(g)=2N2(g)+6H2O(g)дк2LЕФУмБеШнЦїжаНјааЃЌАыЗжжгКѓN2ЕФЮяжЪЕФСПдіМгСЫ0.6molЁЃДЫЗДгІЕФЦНОљЫйТЪІд(XЃЉЮЊ
A.Ід(NH3)ЈT0.04molЁЄLЉ1ЁЄsЉ1B.Ід(O2)ЈT0.015molЁЄLЉ1ЁЄsЉ1
C.Ід(N2)ЈT0.02molЁЄLЉ1ЁЄsЉ1D.Ід(H2O)ЈT0.02molЁЄLЉ1ЁЄsЉ1
ЁОД№АИЁПB
ЁОНтЮіЁП
ИљОн![]() МЦЫуЗДгІЫйТЪЃЌЁїn=0.6molЃЌЁїt=30sЃЌV=2LЃЌдђ
МЦЫуЗДгІЫйТЪЃЌЁїn=0.6molЃЌЁїt=30sЃЌV=2LЃЌдђ![]() ЃЌдкЭЌвЛИіЛЏбЇЗДгІжаЃЌгУВЛЭЌЕФЮяжЪБэЪОЛЏбЇЗДгІЫйТЪЦфЪ§жЕжЎБШЕШгкМЦСПЪ§жЎБШЁЃ
ЃЌдкЭЌвЛИіЛЏбЇЗДгІжаЃЌгУВЛЭЌЕФЮяжЪБэЪОЛЏбЇЗДгІЫйТЪЦфЪ§жЕжЎБШЕШгкМЦСПЪ§жЎБШЁЃ
AЃЎv(NH3): v(N2)=4:2ЃЌдђv(NH3)=2v(N2)= 2ЁС0.01molЁЄLЉ1ЁЄsЉ1=0.02molЁЄLЃ1ЁЄsЃ1ЃЌAДэЮѓЃЛ
BЃЎv(O2): v(N2)=3:2ЃЌдђv(O2)=![]() v(N2)=
v(N2)= ![]() ЁС0.01molЁЄLЉ1ЁЄsЉ1=0.015molЁЄLЃ1ЁЄsЃ1ЃЌBе§ШЗЃЛ
ЁС0.01molЁЄLЉ1ЁЄsЉ1=0.015molЁЄLЃ1ЁЄsЃ1ЃЌBе§ШЗЃЛ
CЃЎv(N2)= 0.01molЁЄLЉ1ЁЄsЉ1ЃЌCДэЮѓЃЛ
DЃЎv(H2O): v(N2)=6:2ЃЌдђv(NH3)=3v(N2)= 3ЁС0.01molЁЄLЉ1ЁЄsЉ1=0.03molЁЄLЃ1ЁЄsЃ1ЃЌDДэЮѓЁЃ
Д№АИбЁBЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПжЦБИЕЊЛЏУОЕФзАжУЪОвтЭМШчЯТЃК
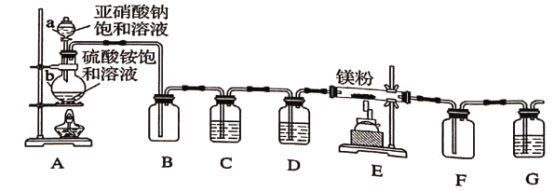
вбжЊЃКAжаЕФЗДгІЃК![]() ЃЌПЩЙЉбЁдёЕФЪдМСЃКХЈСђЫсЁЂМюЪЏЛвЁЂфхЫЎЁЂБЅКЭСђЫсЬњШмвКЁЂБЅКЭСђЫсбЧЬњШмвКЁЂеєСѓЫЎЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЌПЩЙЉбЁдёЕФЪдМСЃКХЈСђЫсЁЂМюЪЏЛвЁЂфхЫЎЁЂБЅКЭСђЫсЬњШмвКЁЂБЅКЭСђЫсбЧЬњШмвКЁЂеєСѓЫЎЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉзАжУDКЭGжаЪЂЗХгаЭЌжжЪдМСЪЧ____ЁЃ
ЃЈ2ЃЉБОЪЕбще§ШЗЕФВйзїЫГађЪЧaЁњdЁњ______ЁњeЁњfЁњiЁЃ
a. АДЭМСЌНгзАжУЃЛb. ЕуШМAДІОЦОЋЕЦЃЛc. зАШыЯргІЪдМСЃЛd. МьВщзАжУЦјУмадЃЛe. ЯЈУ№EДІОЦОЋХчЕЦЃЛ f. РфШДЃЛg. НЋДјЛ№аЧЕФФОЬѕЗХдкGЕМЙмФЉЖЫЃЛh. ЕуШМEДІОЦОЋЕЦЃЛi. ЯЈУ№AДІОЦОЋХчЕЦЃЛ
ЃЈ3ЃЉЧыгУЛЏбЇЗНЗЈШЗЖЈЕЊЛЏУОЪЧЗёКЌгаЮДЗДгІЕФУОЃЌаДГіЪЕбщВйзїМАЯжЯѓ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЭМЪОгыЖдгІЕФа№ЪіЯрЗћЕФЪЧ
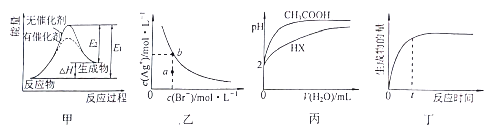
A. ЭММзБэЪОЗХШШЗДгІдкгаЮоДпЛЏМСЕФЧщПіЯТЗДгІЙ§ГЬжаЕФФмСПБфЛЏ
B. ЭМввБэЪОвЛЖЈЮТЖШЯТЃЌфхЛЏвјдкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпЃЌЦфжаaЕуДњБэЕФЪЧВЛБЅКЭШмвКЃЌbЕуДњБэЕФЪЧБЅКЭШмвК
C. ЭМБћБэЪО25ЁцЪБЃЌЗжБ№МгЫЎЯЁЪЭЬхЛ§ОљЮЊ100mLЁЂpH=2ЕФвЛдЊЫсCH3COOHШмвККЭHXШмвКЃЌдђ25ЁцЪБHXЕФЕчРыЦНКтГЃЪ§ДѓгкCH3COOH
D. ЭМЖЁБэЪОФГПЩФцЗДгІЩњГЩЮяЕФСПЫцЗДгІЪБМфБфЛЏЕФЧњЯпЃЌгЩЭМжЊtЪБЗДгІЮязЊЛЏТЪзюДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕШЮяжЪЕФСПЕФ![]() КЭ
КЭ![]() ЕФЛьКЯЮя9.20gгы100mLбЮЫсЗДгІЁЃ
ЕФЛьКЯЮя9.20gгы100mLбЮЫсЗДгІЁЃ
ЃЈ1ЃЉгћЧѓБъзМзДПіЯТЩњГЩ![]() ЕФЬхЛ§ЪБЃЌЛЙашвЊЪВУДЪ§Он_______ЁЃ
ЕФЬхЛ§ЪБЃЌЛЙашвЊЪВУДЪ§Он_______ЁЃ
ЃЈ2ЃЉШє![]() КЭ
КЭ![]() ВЛЪЧЕШЮяжЪЕФСПЛьКЯЃЌдђ9.20gЙЬЬхгыбЮЫсЭъШЋЗДгІЪБЃЌдкБъзМзДПіЯТЩњГЩ
ВЛЪЧЕШЮяжЪЕФСПЛьКЯЃЌдђ9.20gЙЬЬхгыбЮЫсЭъШЋЗДгІЪБЃЌдкБъзМзДПіЯТЩњГЩ![]() ЕФЦјЬхЕФЬхЛ§ЗЖЮЇЃЈVЃЉЮЊ____ЁЃ
ЕФЦјЬхЕФЬхЛ§ЗЖЮЇЃЈVЃЉЮЊ____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙиЛЏбЇгУгяБэЪОе§ШЗЕФЪЧЃЈ ЃЉ
A.ДПМюЕФЛЏбЇЪНЃКNaOH
B.ЗњдзгЕФНсЙЙЪОвтЭМЃК![]()
C.ЙтЕМЯЫЮЌЕФжївЊГЩЗжЃКSi
D.УїЛ§[KAl(SO4)2ЁЄ12H2O]ШмгкЫЎКѓЕФЕчРыЗНГЬЪНЃКKAl(SO4)2=K++Al3++2SO42-
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊЬНОППѓЮяЙЬЬхXЃЈНіКЌ4жжЖЬжмЦкдЊЫиЃЉЕФзщГЩКЭаджЪЃЌЦфжаЙЬЬхввПЩжЦзїЙтЕМЯЫЮЌЁЃЯжЭъГЩШчЯТЪЕбщЃК
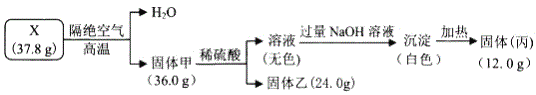
ЧыЛиД№ЃК
ЃЈ1ЃЉXЕФЛЏбЇЪНЮЊ_____ЁЃ
ЃЈ2ЃЉXжаЫљКЌЕФвЛжжН№ЪєдЊЫиЪЧ___ЬюдЊЫиЗћКХЃЉЃЌЦфЕЅжЪдк![]() жаШМЩеЕФЛЏбЇЗНГЬЪНЮЊ_____ЁЃ
жаШМЩеЕФЛЏбЇЗНГЬЪНЮЊ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧыЭъГЩЯТСаЮЪЬтЃК
(1)Cl2КЭЫЎеєЦјЭЈЙ§зЦШШЕФЬПВуЩњГЩHClКЭCO2ЃЌЕБга1 mol Cl2ВЮгыЗДгІЪБЪЭЗХ145 kJШШСПЁЃаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН____________________________ЁЃ
(2)вбжЊCH3OH(l)ЕФШМЩеШШЮЊ238.6 kJЁЄmolЃ1ЃЌCH3OH(l)ЃЋ1/2O2(g) ЃНCO2(g)ЃЋ2H2O(g) ІЄHЃНЃa kJЁЄmolЃ1ЃЌдђa_______238.6(бЁЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁАЃНЁБ)ЁЃ
(3)вбжЊЃКAs(s)+3/2H2(g)+2O2(g)=H3AsO4(s) ІЄH1
H2(g)+1/2O2(g)=H2O(l) ІЄH2
2As(s)+5/2O2(g) =As2O5(s) ІЄH3
дђЗДгІAs2O5(s) +3H2O(l)= 2H3AsO4(s)ЕФІЄH =_________ЁЃ
(4)вбжЊдквЛЖЈЮТЖШЯТЃК
C(s)+ CO2(g)![]() 2CO(g) ЦНКтГЃЪ§K1
2CO(g) ЦНКтГЃЪ§K1
C(s)+ H2O(g)![]() CO(g)+ H2(g) ЦНКтГЃЪ§ K2
CO(g)+ H2(g) ЦНКтГЃЪ§ K2
CO(g)+ H2O(g)![]() H2(g)+ CO2(g)ЦНКтГЃЪ§K3
H2(g)+ CO2(g)ЦНКтГЃЪ§K3
дђK1ЁЂK2ЁЂK3жЎМфЕФЙиЯЕЪЧ__________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТШЛЏбЧЭЪЧгУЭОЙуЗКЕФЭбЮВњЦЗЁЃCuClОЇЬхГЪАзЩЋЃЌЮЂШмгкЫЎЃЌВЛШмгкввДМКЭЯЁбЮЫсЃЌШмгкХЈбЮЫсЃЌМћЙтвзЗжНтЁЃФГбаОПаЁзщвдCuCl2ЃЈКЌЩйСПFe2+ЃЉДжЦЗЮЊдСЯжЦШЁCuClОЇЬхЃЌЩшМЦШчЯТжЦБИСїГЬЃК

ЪЕбщЩцМАЕФВйзїМАзАжУШчЯТЃК

вбжЊ
ЂйдкНЯХЈЕФбЮЫсШмвКжаЃК
a.Cu2+жївЊвд[CuCl4]2-(ГЪЛЦЩЋ)аЮЪНДцдк
b.Fe3+ФмШмНтгкнЭШЁМСвЛМзЛљвьЖЁЛљМзЭЊ(ЮоЩЋЭИУївКЬхЃЌУмЖШЮЊ0.8g/cm3)
ЂкCuClдкШмвКжаДцдкТчКЯгыНтРыЦНКтЃКCuCl(s)+3Cl-(aq)![]() [CuCl4]3-(aqЮоЩЋ)
[CuCl4]3-(aqЮоЩЋ)
ЂлSOCl2ШлЕу-105ЁцЁЂЗаЕу76ЁцЁЂгіЫЎОчСвЫЎНтЩњГЩSO2КЭHClЦјЬх
ЧыЛиД№ЃК
(1)ЯТСагаЙиCuCl2ЬсДПВйзїе§ШЗЕФЪЧ______
A.НЋбѕЛЏвКзЊвЦжСЗжвКТЉЖЗжаЃЌМгШынЭШЁМСКѓЃЌШћЩЯВЃСЇШћЃЌгУСІеёвЁЃЈМћЩЯЭМ1ЃЉ
B.ОМИДЮеёвЁВЂДђПЊЩЯПкВЃСЇШћЗХЦјКѓЃЌНЋЗжвКТЉЖЗжУгкЬњМмЬЈЕФЬњШІЩЯЃЌОВжУЦЌПЬ
C.Fe2+ОбѕЛЏЁЂнЭШЁЁЂЗжвКЃЌНјШыгаЛњЯрГ§ШЅ
D.ШЁЗжвККѓЕФЫЎЯрЩйаэЃЌЕЮШыKSCNШмвКМьбщнЭШЁЪЧЗёЭъШЋ
(2)ЛЙдЗДгІзАжУШчЩЯЭМ2ЫљЪОЃК
ЂйЯђШ§ОБЩеЦПжаЛКТ§ЕЮМгSOCl2ЪБЃЌашДђПЊЛюШћ_____ЃЈЬюЁАaЁБЁЂЁАbЁБЛђЁАaКЭbЁБЃЉЁЃ
ЂкЫЎЯржа[CuCl4]2-БЛSOCl2ЛЙдЮЊ[CuCl4]3-ЕФРызгЗНГЬЪНЮЊ______ЁЃ
ЂлХаЖЯЗДгІЭъГЩЕФЪЕбщЯжЯѓЪЧ________________ЁЃ
(3)ЯђЛьКЯвКжаМгШыДѓСПШЅбѕЫЎФмЕУЕНCuC1аќзЧвКЕФдвђЪЧ___________
(4)ЁАЯЕСаВйзїЁБАќРЈЃКГщТЫЁњЯДЕгЁњИЩдяЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ__________
A.ГщТЫВйзїгУЕНЕФЦїВФАќРЈТЫжНЁЂВМЪЯТЉЖЗЁЂЮќТЫЦПЁЂАВШЋЦПКЭГщЦјБУЕШ
B.ПЩбЁгУЮоЫЎввДМЯДЕгCuClЃЌЯДЕгЪБгІЙиБеЫЎСњЭЗЃЌЪЙЯДЕгМСЛКТ§ЭЈЙ§ГСЕэЮя
C.ШЁзюКѓвЛДЮЯДЕгвКЃЌЕЮМгBaCl2ШмвКЃЌШєЮоАзЩЋГСЕэВњЩњЃЌдђжЄУїВњЦЗвбЯДОЛ
D.дкБмЙтЯТВњЦЗгІжУгкAДІецПеИЩдя(ЩЯЭМ3)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЭЌбЇгћХфжЦ450mL 0.5mol/LЕФЧтбѕЛЏФЦШмвКЃЌЧыЛиД№ЯТСаЮЪЬтЃК
(1)зМШЗГЦШЁЧтбѕЛЏФЦЕФжЪСП______ЁЃ
(2)дкХфжЦЙ§ГЬжаЃЌВЛЛсгУЕНЕФЪЕбщвЧЦїЪЧ______(ЬюзжФИ)ЁЃ
A.500mLШнСПЦПB.ЭаХЬЬьЦНC.дВЕзЩеЦПD.ЩеБE.ВЃСЇАєF.зЖаЮЦП
Г§ЩЯЪівЧЦїЭтЃЌЩаШБЕФВЃСЇвЧЦїЪЧ______
(3)ХфжЦЧтбѕЛЏФЦШмвКЪБЃЌЯТСаВйзїПЩФмЛсЪЙЫљХфШмвКЮяжЪЕФСПХЈЖШЦЋЕЭЕФЪЧ______
AЃЎЫљгУNaOHЙЬЬхвбГБНт
BЃЎШнСПЦПЕзгаЩйСПеєСѓЫЎ
CЃЎзЊвЦШмвКЙ§ГЬжагаЩйСПвКЬхНІГі
DЃЎЖЈШнЪБИЉЪгЖСЪ§
EЃЎЖЈШнвЁдШКѓЃЌвКУцЕЭгкПЬЖШЯпЃЌМЬајЕЮМгеєСѓЫЎжСПЬЖШЯп
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com