
【题目】CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是

A. 该反应的ΔH<0
B. 在500℃条件下达平衡时CO 的转化率为60%
C. 平衡常数K1(3000C)<K2(5000C)
D. 图2中达化学平衡的点为c、d、e
【答案】C
【解析】
根据图1,随着温度升高,甲醇的物质的量减小,根据勒夏特列原理,该反应为放热反应,根据图2,当反应达到平衡时,甲醇的物质的量最大,依据化学平衡移动的定义,推出c、d、e达到平衡;
A、根据图1,300℃时,甲醇物质的量为0.8mol,500℃时甲醇物质的量为0.6mol,升高温度,向正反应方向移动,根据勒夏特列原理,该反应为放热反应,即△H<0,故A说法正确;
B、500℃时甲醇的物质的量为0.6mol,则消耗CO的物质的量为0.6mol,即CO的转化率为0.6mol/1mol×100%=60%,故B说法正确;
C、化学平衡常数只受温度的影响,该反应为放热反应,升高温度,平衡向逆反应方向进行,即化学平衡常数减小,即K1(300℃)>K2(500℃),故C说法错误;
D、a到c反应向正反应方向进行,还没有达到平衡,当达到平衡时,甲醇的物质的量最多,即c、d、e为化学平衡点,故D说法正确;


科目:高中化学 来源: 题型:
【题目】H2、N2合成NH3的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
A. v(N2)=0.6mol/(L·min)B. v(NH3)=0.9mol/(L·min)
C. v(H2)=1.2mol/(L·min)D. v(H2)=0.025mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钙晶体(CaC2O4·H2O)是一种受热容易分解的盐,某班同学要探究其受热分解的产物,甲组同学认为其分解产物可能是CaCO3、CO和H2O,乙组同学认为其分解产物可能是CaO、CO2和H2O。两组同学将草酸钙晶体放入石英试管进行加热,按照下图所示装置进行探究,请回答相关问题。
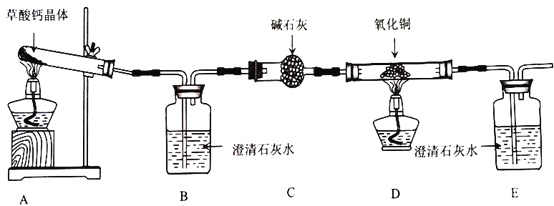
(1)盛放碱石灰的仪器名称是___________。证明分解产物中有CO的现象是______________________。
(2)装置存在一处明显缺陷,该缺陷是________________,改进的方法是______________________(任写一种)。
(3)实验中B中澄清石灰水未变浑浊,甲组同学认为自己的判断正确,但乙组同学认为可能是因为温度不够,需将试管下方酒精灯更换为___________重新实验。
(4)更换仪器及各种试剂后重新实验,B中澄清石灰水变浑浊,装置C的作用是______________________。
(5)更换仪器重新实验时发生的反应方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以钙为例,用化学方程式表示钙及其化合物之间的转化关系。

(1)①______________________________________________。
②______________________________________________。
③______________________________________________。
④______________________________________________。
⑤______________________________________________。
⑥______________________________________________。
(2)上述反应中,属于化合反应的是______(填序号,下同),属于复分解反应的是_____。
(3)上述反应①~⑥中属于氧化还原反应的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态砷原子的价电子排布式为____。
(2)氟、氧、砷三种元素的电负性由大到小的顺序是____(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反:Fe(SCN)3+6NH4F=== (NH4)3FeF6+3NH4SCN
①NH4F 中阳离子的立体构型为____。
②(NH4)3FeF6存在的微粒间作用力有__(选填序号,下同)。
a.离子键 b.共价键 c.金属键 d.配位键 e.范德华力 f.氢键
③已知SCN中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为____,该原子团中σ与π键个数比为____。
(4)FeCl3晶体易溶于水、乙醇,受热易气化,而FeF3晶体熔点高于1000oC,试解释两种化合物熔点差异较大的原因:____。
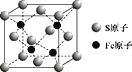
(5)S和Fe形成的某化合物,其晶胞如图所示,则该物质的化学式为 ___。设该晶胞的密度为ρ g/cm3,用NA表示阿伏加德罗常数,则该晶胞中距离最近的S原子之间的距离为(列出计算式即可)____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氯元素全部被氧化的是( )
A. 2P+3Cl2![]() 2PCl3
2PCl3
B. 2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
C. NaOH+HClNaCl+H2O
D. 2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列方法均可制得氯气:
①MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A. 6∶5∶6B. 1∶3∶5C. 15∶5∶3D. 1∶6∶10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别由短周期元素m、n、p、q组成的单质依次为甲、乙、丙、丁,有关反应关系如图所示(部分产物省略)。其中甲为黄绿色气体,M、N均为10电子分子且M的水溶液呈碱性,Q为离子化合物,下列说法中正确的是

A. 原子半径的大小m>q>n>p
B. 元素非金属性q>n>p
C. Q的溶液可以保存在细口玻璃试剂瓶
D. n的氧化物的水化物一定为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中烃的分子式排列规律,判断空格中的烃的同分异构体数目( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A. 2B. 3C. 4D. 5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com