
����Ŀ��CO2��һ�ֳ������������壬�������պ�����Ҳ��Ϊ�ִ��Ƽ������ſ��⡣
(1)�����ܱ������У���Cu/ZnO���������£�����CO2�Ʊ��״���CO2(g) + 3H2(g)CH3OH(g) + H2O(l) ��H1����֪�� CH3OH(g) +![]() O2(g)=CO2(g) + 2H2O(l) ��H2��д������ȼ���ȵ��Ȼ�ѧ����ʽ________(��H�á�H1�� ��H2��ʾ)��ij�¶��£������Ϊ2L���ܱ������м���2mol CO2��5mol H2�Լ��������з�Ӧ����CH3OH ������ˮ�������ﵽƽ��ʱH2��ת������60%����ƽ�ⳣ��Ϊ_______��
O2(g)=CO2(g) + 2H2O(l) ��H2��д������ȼ���ȵ��Ȼ�ѧ����ʽ________(��H�á�H1�� ��H2��ʾ)��ij�¶��£������Ϊ2L���ܱ������м���2mol CO2��5mol H2�Լ��������з�Ӧ����CH3OH ������ˮ�������ﵽƽ��ʱH2��ת������60%����ƽ�ⳣ��Ϊ_______��
(2)��ҵ����CO2��������ȡ�����ѣ�2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)����������ͬ�ĺ����ܱ������У���������ķ�Ӧ��ֱ���Ir��Ce����������Ӧ������ͬ��ʱ����õ�CO2��ת������(CO2)�淴Ӧ�¶ȵı仯�����ͼ��ʾ��
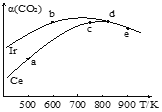
����Ir��Ce������ʱ����Ӧ�Ļ�ܸ��͵���_________��
��a��b��c��d��e����״̬����Ӧһ���ﵽƽ��״̬����________����Ӧ����H ____0(���������=������)��
�۴�״̬a��c��CO2ת���ʲ��������ԭ����__________��
����֪T���£���2 molCO2��6 molH2ͨ�뵽���ΪV L���ܱ������н���������Ӧ����Ӧʱ���������ڵ���ѹǿ���������
ʱ��t/min | 0 | 10 | 20 | 30 | 40 |
��ѹǿp/1000kPa | 1.0 | 0.83 | 0.68 | 0.60 | 0.60 |
�÷�Ӧƽ��ʱCO2��ת����Ϊ___________��
(3)��ҵ�ϳ��ð�ˮ���պ�̼ȼ��ȼ���в�������������CO2���õ�NH4HCO3��Һ����ӦNH4++HCO3��+H2ONH3��H2O+H2CO3��ƽ�ⳣ��K=_________��(��֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10��5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10��7��Ka2=4��10��11 )��
���𰸡�H2 (g) +![]() O2 (g)=H2O(l) ��H=(��H1+ ��H2)/3 0.5 Ir d��e �� ״̬a��c��δ�ﵽƽ�⣬״̬c�¶ȸ߷�Ӧ���ʿ죬CO2��ת������ת���ʸ� 80% 1.25��10��3
O2 (g)=H2O(l) ��H=(��H1+ ��H2)/3 0.5 Ir d��e �� ״̬a��c��δ�ﵽƽ�⣬״̬c�¶ȸ߷�Ӧ���ʿ죬CO2��ת������ת���ʸ� 80% 1.25��10��3
��������
(1)��֪��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l) ��H1����CH3OH(g)+
CH3OH(g)+H2O(l) ��H1����CH3OH(g)+![]() O2(g)
O2(g)![]() CO2(g)+2H2O(l) ��H2���ɸ�˹���ɼ���(��+��)��
CO2(g)+2H2O(l) ��H2���ɸ�˹���ɼ���(��+��)��![]() �õ�����ȼ���ȵ��Ȼ�ѧ����ʽ��H2(g)+
�õ�����ȼ���ȵ��Ȼ�ѧ����ʽ��H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ��H=
H2O(l) ��H=![]() (��H1+��H2)��ij�¶��£������Ϊ2L���ܱ������м���2mol CO2��5molH2�Լ��������з�Ӧ����CH3OH������ˮ�������ﵽƽ��ʱH2��ת������60%�������������ʵ���Ũ��=2.5mol/L��60%=1.5mol/L��������ʽ�У�
(��H1+��H2)��ij�¶��£������Ϊ2L���ܱ������м���2mol CO2��5molH2�Լ��������з�Ӧ����CH3OH������ˮ�������ﵽƽ��ʱH2��ת������60%�������������ʵ���Ũ��=2.5mol/L��60%=1.5mol/L��������ʽ�У�
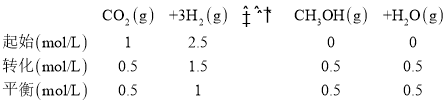
��ƽ�ⳣ��![]() ���ʴ�Ϊ��H2(g)+
���ʴ�Ϊ��H2(g)+![]() O2(g)
O2(g)![]() H2O(l)
H2O(l) ![]() (��H1+��H2)��0.5��
(��H1+��H2)��0.5��
(2)�ٸ���ͼʾ��Ϣ���ֱ���Ir��Ce����������Ӧ������ͬ��ʱ����õ�CO2��ת����a(CO2)�淴Ӧ�¶ȵı仯������õ���CO2��ת����a(CO2)�ߣ�������Ч�ʸߣ���ܽ�С��������Ir��Ce������ʱ����Ӧ�Ļ�ܸ��͵���Ir���ʴ�Ϊ��Ir��������Ӱ��ת���ʣ�a��b��c��d��e����״̬����Ӧ�ﵽƽ��״̬ʱ��CO2��ת����a(CO2)���ٱ仯����ƽ��״̬��d��e���ﵽƽ���Ժ��¶����ߣ�CO2��ת����a(CO2)��С������ƽ�������ƶ�����Ӧ�Ƿ��ȷ�Ӧ�����Է�Ӧ���ʱ�С���㣬�ʴ�Ϊ��d��e������
��״̬a��c��δ�ﵽƽ�⣬״̬c�¶ȸ߷�Ӧ���ʿ죬CO2��ת������ת���ʸߣ��ʴ�Ϊ��״̬a��c
��T���£���2molCO2��6molH2ͨ�뵽���ΪVL���ܱ������н���������Ӧ��ͼ�����ݿ�֪��ƽ��״̬����ѹǿ����0.4KPa�������ɶ��������ʵ���Ϊx mol��������ʽ�У�
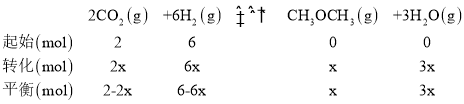
���ݰ����ӵ�����PV=nRT������ѹǿ֮�ȵ����������ʵ���֮�ȣ���![]() ����x=0.8��ƽ��ʱCO2��ת����
����x=0.8��ƽ��ʱCO2��ת����![]() ���ʴ�Ϊ��80%��
���ʴ�Ϊ��80%��
(3)��ӦNH4++HCO3��+H2ONH3��H2O+H2CO3��ƽ�ⳣ�� ���ʴ�Ϊ��1.25��10��3��
���ʴ�Ϊ��1.25��10��3��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ����й㷺�Ŀ�����Ӧ��ǰ����������ɱ���ܱ�������Ͷ��0.5molCO��1molH2����ͬ�����·�����Ӧ��CO(g)+2H2(g)![]() CH3OH(g)��ʵ����ƽ��ʱCH3OH�����ʵ������¶ȡ�ѹǿ�ı仯��ͼ1��ʾ������˵����ȷ����
CH3OH(g)��ʵ����ƽ��ʱCH3OH�����ʵ������¶ȡ�ѹǿ�ı仯��ͼ1��ʾ������˵����ȷ����
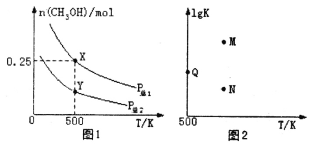
A.P��1<P��2
B.���������ܶȲ��ٷ����仯��˵���÷�Ӧ�Ѵﵽƽ��״̬
C.ͼ2��M������ȷ��ʾ�÷�Ӧƽ�ⳣ���Ķ���(1gK)���¶ȵĹ�ϵ
D.��P��1=0.25MPa����Y���ƽ�ⳣ��Kp=64(MPa)-2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ�û�ʵ�������ȷ����

A. ����pH��ֽ��ij��Һ������� B. ��̽�������ԣ�KMnO4>Cl2>I2
C. �����հ����ư�ˮ D. ���к͵ζ�ʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G�����ʼ�Ĺ�ϵ��ͼ������B��DΪ��̬���ʡ�

��ش��������⡣
(1)����C��E�����Ʒֱ�Ϊ_______��_______��
(2)��ѡ�ò�ͬ��A���з�Ӧ���������ڳ����½��У��仯ѧ����ʽΪ___________________����ֻ���ڼ�������½��У���Ӧ��AӦΪ_______��
(3)MnO2�ڷ�Ӧ���ͷ�Ӧ���е����÷ֱ���_______��_______��
(4)�����Ƶ�F��ҺӦ����_______�Է�ֹ��ת��ΪG������G��Һ�������ӵij����Լ���_______��ʵ������Ϊ_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ʵ����ܷ�����ѧ��Ӧ��
�� | �� | �� |
��������������ͭ��Һ�� | ������������Һ�е��뼸����ˮ | ��ͭ˿�����Ȼ�����Һ�� |
�����ж���ȷ����
A.ʵ�����������ԭ��B.ʵ�����![]() �������������Ի�ԭ��
�������������Ի�ԭ��
C.ʵ����з��������û���ӦD.����ʵ��֤��������:![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»����

����˵����ȷ���ǣ� ��
A.����������ķ���ʽΪC4H8B.�������������ȡ��������1��
C.������ϩ�˴Ź���������2���D.������ϩ�뱽��Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���һ���������ڲ���һ����©���ҿ��Ի����Ļ������������ָ���������ҡ����ҳ���N2�����ҳ���H2��O2����������ʹN2ռ���������![]() ����ͼ����
����ͼ����
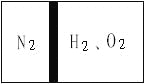
Ȼ���ȼH2��O2�Ļ�����壬��Ӧ��Ϻ�ָ���ԭ�����¶ȣ���������ͣ�����������м䡣�����飬��ʱ�����������ʹ�����ǵ�ľ����ȼ����ӦǰH2��O2�����ʵ���֮��Ϊ___�������Ҫд��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��Ũ�Ⱦ�Ϊ0.5 mol/L��(NH4)2SO4��(NH4)2CO3��(NH4)2Fe(SO4)2��������Һ����ø���Һ��c(NH4+)�ֱ�Ϊa��b��c(��λΪmol/L)�������ж���ȷ����
A.a=b=cB.a��b��cC.a��c��bD.c��a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڻ�ѧ��ҵ�����ż���㷺��Ӧ�á�
��1����1.25mol��NO��NO2��N2O4��������NO���������Ϊ0.60��ͨ��ˮ�У��ڿ����������������ȫ��Ӧ��ɻ����������ʵ�����Χ��_______________��
��2����ϡ�����м���18.4mol/L��Ũ���ᣨ98%������ˮ���������Ũ���ᣬ����Ũ���½���87%���ܶ�1.8g/cm3������ʱ����ʧȥ��ˮ������50mL 18.4mol/L��Ũ������Ϊ��ˮ��ʱ��������ˮ_________ g��
��3����65%��HNO3������m1���м���72%��Mg(NO3)2������m2�������ֱ�õ�97.5%��HNO3��60%��Mg(NO3)2��Һ�����в������ᣩ������������У����ᡢ����þ������ģ�H2O�����ռ��������5%��������ǰͶ�ϱ�![]() ��______________��
��______________��
��4�����Ṥҵ�е�β�����ռ�������ղ���ΪNaNO2��NaNO3��H2O�����к�0.50mol���������β����ǡ�ñ�һ������NaOH��Һ��ȫ���ա���֪��Ӧ����Һ����0.35mol��NaNO2������β��NO��NO2��ƽ�������NOx��ʾ����x =___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com