
| A、强电解质都是离子化合物,弱电解质都是共价化合物? |
| B、强电解质都是可溶性化合物,弱电解质都是难溶性化合物? |
| C、强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子? |
| D、强电解质的水溶液导电能力强,弱电解质的水溶液导电能力弱? |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
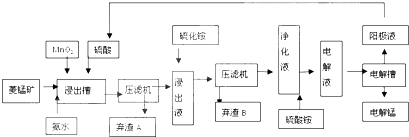
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 |
| 难溶物质 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | NiS | CoS |
| pKsp | 38.55 | 15.26 | 14.7 | 18.49 | 20.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3 | B、4 | C、5 | D、6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时溶液中一定大量共存:Na+、Ca2+、Cl-、SO42- |
| B、能与铝反应放出氢气的溶液中一定共存:Mg2+、Cu2+、SO42-、NO3- |
| C、弱碱性溶液中可能大量共存:Na+、K+、Cl?、HCO3? |
| D、0.1mol/LFeCl3溶液中可能大量共存:Fe2+、NH4+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5a=2b |
| B、2a=5b |
| C、3a=2b |
| D、2a=3b |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.
短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.| X | |||
| Z | W | Y |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将纯水加热到99℃ |
| B、向水中加少量AlCl3固体 |
| C、向水中加入一小粒金属钠 |
| D、向水中加少量NaOH固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com