
���� ��1��������Һϡ�������������ʵ����ʵ������������ҪŨ���������
��2����������һ�����ʵ���Ũ����Һһ�㲽��ѡ����Ҫ������
��3�����ݷ���ʽ����μӷ�Ӧ��п���Ȼ�������ʵ���������m=nM����������������Ӧ�����Һ�м���100mLNaOH��Һǡ��ʹ��Ԫ����ȫ����������������ȫ��ת��Ϊ�Ȼ��ƣ�������ԭ�Ӹ����غ���㣮
��� �⣺��1������ҪŨ�������ΪV����������Һϡ�������������ʵ����ʵ�������ã�10moL/L��V=250mL��1mol/L�����V=25.0mL��
�ʴ�Ϊ��25.0��
��2������һ�����ʵ���Ũ����Һһ�㲽��Ϊ�����㡢��ȡ��ϡ�͡���Һ��ϴ�ӡ����ݣ��õ�����������Ͳ���ձ�����������250mL����ƿ����ͷ�ιܣ��������õ���������250mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��250mL����ƿ����ͷ�ιܣ�
��3��Fe+2HCl=FeCl2+H2��
1mol 2mol 22.4L
x y 0.896L
���x=$\frac{0.896L}{22.4L}$=0.04mol��������������m=0.04mol��56g/mol=2.24g��
��Ӧ�����Һ�м���100mLNaOH��Һǡ��ʹ��Ԫ����ȫ����������������ȫ��ת��Ϊ�Ȼ��ƣ�������ԭ�Ӹ����غ�ã�n��HCl��=n��NaOH������100mL��1mol/L=100mL��C��NaOH��
���C��NaOH��=1mol/L��
�ʴ�Ϊ��1mol/L��
���� ���⿼����һ�����ʵ���Ũ����Һ�����Ƽ��йط���ʽ�ļ��㣬��ȷ����ԭ��������ʽ�и�����֮�����Ĺ�ϵ�ǽ���ؼ�����Ŀ�ѶȲ���


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
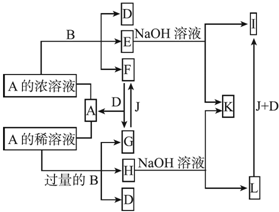
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Al�ܷų�H2����Һ�У�ClO-��HCO${\;}_{3}^{-}$��SO${\;}_{4}^{2-}$��NH${\;}_{4}^{+}$ | |
| B�� | pH=2����Һ�У�Fe2+��Na+��Mg2+��NO${\;}_{3}^{-}$ | |
| C�� | ��ʹKSCN��Һ������Һ�У�Na+��I-��NO${\;}_{3}^{-}$��HCO${\;}_{3}^{-}$ | |
| D�� | ��ˮ�������c��OH-��=1.0��10-13mol•L-1����Һ�У�Na+��Ba2+��Cl-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
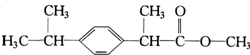 ij��ҩ����Ҫ�ɷ�X�ķ��ӽṹ��ͼ�������л���X��˵���д�����ǣ�������
ij��ҩ����Ҫ�ɷ�X�ķ��ӽṹ��ͼ�������л���X��˵���д�����ǣ�������| A�� | �٢� | B�� | �ڢ� | C�� | �ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
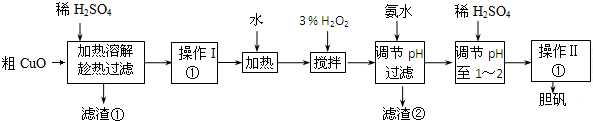
| Fe3+ | Fe2+ | Cu2+ | |
| �������↑ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
| �������������ȫʱ��pH | 3.2 | 9.0 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ����ʽ | ��� | �ȷֽ��¶� | �۵� | �ܽ��� |
| CO��NH2��2•H2O2 | ��ɫ���� | 45�� | 75-85�� | ������ˮ���л��ܼ� |
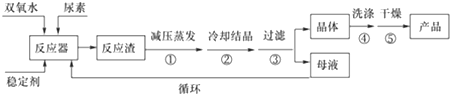
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��Һ�У����ܺ����±����������е�ij���֣�
ij��Һ�У����ܺ����±����������е�ij���֣�| ������ | Al3+��Mg2+��NH4+��Na+ |
| ������ | CO32-��SiO32-��[Al��OH��4]-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com