
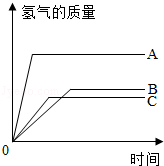
分析 由图可知,反应时间少的反应最快,则金属最活泼,均为二价金属,结合n(H2)×2=$\frac{m}{M}$×(2-0)可知,M=$\frac{m}{n({H}_{2})}$,以此分析相对原子质量大小.
解答 解:金属A的反应速度最快,活动性最大,金属B的反应速度最慢,活动性则最小,则时间B>C>A,则金属活泼性为A>C>B;
根据反应情况图,在停止反应前的同一时间,由n(H2)×2=$\frac{m}{M}$×(2-0)可知,M=$\frac{m}{n({H}_{2})}$,三种金属产生氢气质量从大到小的顺序为A>B>C,则质量相同时相对原子质量大小的顺序是C>A>B,
故答案为:A>C>B;C>A>B.
点评 本题考查金属活泼性比较,侧重于学生的分析能力的考查,为高考常见题型,注意把握图象中生成氢气的速率及M的比较方法为解答该类题目的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

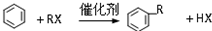 A具有和苯相似的性质.
A具有和苯相似的性质. 2HCHO+2H2O;
2HCHO+2H2O;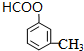 、
、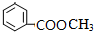 ;
;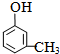 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
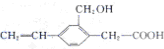
| A. | 该有机化合物的分子式为C11H10O3 | |
| B. | 该有机化合物能发生取代反应、加成反应和加聚反应 | |
| C. | 1mol该有机化合物分别消耗Na、NaOH和NaHCO3的物质的量之比为2:2:1 | |
| D. | 该有机化合物与 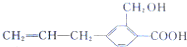 互为同系物 互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500℃左右的温度比室温更有利于合成氨反应N2(g)+3H2(g)?2NH3(g)△H<0 | |
| B. | 在恒容密闭容器中充入一定量NO2建立2NO2(g)═N2O4(g)△H<0 平衡后,升高温度,体系颜色加深 | |
| C. | 向水中投入金属Na,最终溶液呈碱性 | |
| D. | FeCl3和KSCN的混合溶液中加入FeCl3固体,溶液颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3↓+3H+ | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,正极反应式为:Cu-2e-═Cu2+ | |
| D. | NaHS水解:HS-+H2O?H3O++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | >0.1mol/L | B. | <0.1mol/L | C. | 0.1mol/L | D. | 不能确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com