
【题目】按纯净物、混合物、强电解质顺序排列的一组物质是
A.盐酸、空气、醋酸B.液氯、海水、硫酸钠C.铁粉、碘盐、碳酸D.胆矾、漂白粉、氯化钾溶液
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】新合成的一种烃,其碳架呈三棱柱体(如图所示):

(1)写出该烃的分子式_________________________。
(2)该烃的一氯取代物是否有同分异构体_________。
(3)该烃的二氯取代物有多少种_________________。
(4)该烃的同分异构体有多种,其中1种不能使酸性高锰酸钾溶液或Br2-CCl4溶液褪色,但在一定条件下能跟溴(或H2)发生取代(或加成)反应,这种同分异构体的结构简式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(g)和H2O(g)以1 : 2体积比分别通入到体积为2 L的恒容密闭容器中进行反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:

下列说法不正确的是
A. 从实验数据分析,该反应的正反应是吸热反应
B. 实验A中,在0~10min内,以v(H2)表示的反应速率大于0.013mol(L·min)-1
C. 从生产效益分析,C组实验的条件最佳
D. 比较实验B、C,说明C实验使用了更高效的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的是( )


A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以原油为原科生产聚烯烃的流程如下:

回答下列问题:
(1)流程中②表示的加工方法是_____(填序号)。
A.分馏 B.分液 C.裂解 D.干馏
(2)C4~C10的混合物中含戊烷,请写出戊烷的所有同分异构体的结构简式:______。
(3)聚乙烯的结构简式为______。
(4)丙烯与乙烯化学性质相似。丙烯可以与水反应生成丙醇,该反应类型是____,丙醇中官能团的名称是____。
(5)写出乙醇催化氧化生成乙醛的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应:2NaClO2 + Cl2 ===2ClO2 + 2NaCl。
下图是实验室用于制备和收集一定量较纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体(用于除去ClO2中的未反应的Cl2)。

(1)仪器P的名称是______。
(2)写出装置A中烧瓶内发生反应的离子方程式:_________。
(3)B装置中所盛试剂是_____,G瓶的作用是_______。
(4)F为ClO2收集装置,应选用的装置是____(填序号),其中与E装置导管相连的导管口是_____(填接口字母)。

(5)若用100 mL 2 mol·L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是_____(填序号)。
A.>0.1mol B.0.1 mol C.<0.1 mol D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是 ( )
A. 分子中三个碳原子可能处于同一直线上
B. 全氟丙烷(C3F8)的电子式为: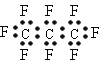
C. 相同压强下,沸点:C3F8<C3H8
D. 全氟丙烷(C3F8)分子中既有极性键又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲烷分子中C原子sp3杂化轨道电子云图:

(1)请你在图中画出甲烷分子中H原子的电子云图。甲烷分子中C-H键的键角为_______________;
(2)乙烯和乙炔的电子式分别为______________、______________,请你比较乙烯和乙炔分子中“C=C”和“C≡C”的键长大小:___________________________。乙炔和乙烯一样都能和溴水发生加成反应并使溴水褪色,请你预测在同浓度同体积的溴水中分别通入乙烯和乙炔时,_____________(选填“乙烯”、“乙炔”)使溴水褪色的时间短;同温同压下,使等体积等浓度的溴水正好褪色,消耗的______________(选填“乙烯”、“乙炔”)少;
(3)苯分子中C原子以sp2杂化成键,6个C原子中每个C原子2s轨道和其中2个2p轨道形成3个sp2杂化轨道,其中1个sp2杂化轨道与1个H原子形成1个σ键、另外2个sp2杂化轨道分别与另外2个C原子的sp2杂化轨道形成2个σ键而形成1个六元环,而每个C原子未参与杂化的另1个2p轨道均垂直于这个六元环所处的平面并相互之间“肩并肩”重叠形成1个“大π键”,如下图:

请你猜想:
① 苯分子中每个碳碳键的键长是否相等?______________________;
② 苯分子中碳碳键的键长与C-C单键、C=C双键、C≡C叁键的键长相比,处于_______________________________________的键长之间。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com