
【题目】磷酸是三元弱酸,常温下三级电离常数分别是:Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:
(1)常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序___(填序号)。
(2)常温下,NaH2PO4的水溶液pH___(填“>”“<”或“=”)7。
(3)常温下,Na2HPO4的水溶液呈___(填“酸”“碱”或“中”)性,用Ka与Kh的相对大小,说明判断理由:__。
【答案】③<②<① < 碱 Na2HPO4的水解常数Kh=![]() =
=![]() =
=![]() ≈1.61×10-7,Kh>Ka3,即HPO4-的水解程度大于其电离程度,因而Na2HPO4溶液显碱性
≈1.61×10-7,Kh>Ka3,即HPO4-的水解程度大于其电离程度,因而Na2HPO4溶液显碱性
【解析】
(1)①Na3PO4中PO43-的水解平衡常数是![]() 、②Na2HPO4中HPO42-水解平衡常数是
、②Na2HPO4中HPO42-水解平衡常数是![]() ;③NaH2PO4中H2PO4-水解平衡常数是
;③NaH2PO4中H2PO4-水解平衡常数是![]() ,水解常数依次减小,所以pH由小到大的顺序③<②<①;
,水解常数依次减小,所以pH由小到大的顺序③<②<①;
(2)NaH2PO4中H2PO4-水解平衡常数是![]() ,电离常数是Ka2=6.2×10-8,H2PO4-的电离大于水解,溶液呈酸性,pH<7;
,电离常数是Ka2=6.2×10-8,H2PO4-的电离大于水解,溶液呈酸性,pH<7;
(3)Na2HPO4的水解常数Kh=![]() =
=![]() =
=![]() ≈1.61×10-7,Kh>Ka3,即HPO4-的水解程度大于其电离程度,因而Na2HPO4溶液显碱性。
≈1.61×10-7,Kh>Ka3,即HPO4-的水解程度大于其电离程度,因而Na2HPO4溶液显碱性。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有机反应方程式书写正确且为加成反应的是( )
A.CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B.CH2=CH2+Br2→CH3-CHBr2
C.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
D.![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用元素周期律分析下面的推断,其中错误的是![]()
A.铍![]() 的氧化物对应的水化物可能具有两性
的氧化物对应的水化物可能具有两性
B.砹![]() 为有色固体,HAt不稳定,AgAt感光性很强,且不溶于水也不溶于酸
为有色固体,HAt不稳定,AgAt感光性很强,且不溶于水也不溶于酸
C.硒化氢![]() 是无色、有毒且稳定性比硫化氢还差的气体
是无色、有毒且稳定性比硫化氢还差的气体
D.同一主族的元素从上到下,金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,配制一组c(H2A)+c(HA-)+c(A2-)=0.10mol·L-1的H2A和NaOH的混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法中正确的是( )
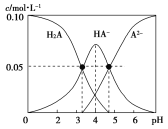
A.在c(Na+)=0.10mol·L-1的溶液中:c(A2-)-c(H+)=c(H2A)-c(OH-)
B.pH=4的溶液中:c(HA-)=c(H2A)+c(A2-)
C.pH=7的溶液中:c(Na+)=c(A2-)+c(HA-)
D.Ka1(H2A)的数量级为10-5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质与条件已略去,其中反应②的条件是“700 ℃,催化剂”)。G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体。
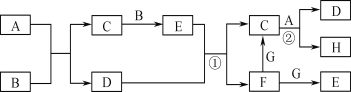
请回答下列问题:
(1)E的化学式为________________。
(2)A的电子式为________________。
(3)写出反应①的离子方程式:________________________________。
(4)写出反应②的化学方程式,并标出电子转移的方向与数目:
______________ __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请阅读下列材料,回答下列小题。
铁放置时间长了就会生锈。铁容易生锈,除了由于它的化学性质活泼以外,同时与外界条件也有很大关系。水分是使铁容易生锈的物质之一。然而,光有水也不会使铁生锈,只有当空气中的氧气溶解在水里时,氧在有水的环境中与铁反应,才会生成一种叫氧化铁的东西,这就是铁锈,铁生锈总的反应为4Fe+3O2+xH2O![]() 2Fe2O3·xH2O。铁锈是一种棕红色的物质,它不像铁那么坚硬,很容易脱落,一块铁完全生锈后,体积可胀大8倍。如果铁锈不除去,这海绵状的铁锈特别容易吸收水分,铁也就锈蚀的更快了。
2Fe2O3·xH2O。铁锈是一种棕红色的物质,它不像铁那么坚硬,很容易脱落,一块铁完全生锈后,体积可胀大8倍。如果铁锈不除去,这海绵状的铁锈特别容易吸收水分,铁也就锈蚀的更快了。
【1】铁生锈总反应属于 ( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
【2】关于反应4Fe(OH)2+O2+2H2O![]() 4Fe(OH)3,下列说法正确的是 ( )
4Fe(OH)3,下列说法正确的是 ( )
A.O2发生还原反应
B.Fe(OH)2被还原
C.H2O发生氧化反应
D.H2O是氧化剂
【3】下列反应条件的改变对4Fe+3O2+xH2O![]() 2Fe2O3·xH2O速率的影响不正确的是( )
2Fe2O3·xH2O速率的影响不正确的是( )
A.增大O2的浓度能加快生锈速率
B.潮湿环境中铁生锈的速率更快
C.升高温度能加快生锈速率
D.干燥空气中铁生锈速率更快
【4】下列反应吸收热量的是 ( )
A.铁与稀盐酸反应
B.铁丝在氧气中燃烧
C.铝还原氧化铁
D.碳与二氧化碳反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A、B、C分别是三种有机物的结构模型:
A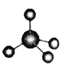 B
B C
C
请回答下列问题:
(1)上述三种模型最能真实体现有机物空间构型的是_____(填序号)。
(2)B及其同系物的分子式符合通式____(用n表示)。当n=_____时,烯烃开始出现同分异构体。
(3)有机物C中,共直线的的原子有_______个。
(4)有机物C具有的结构或性质是______(填字母序号)。
a .是碳碳双键和碳碳单键交替的结构 b. 有毒、不溶于水、密度比水小
c. 不能使酸性KMnO4溶液和溴水褪色 d. 一定条件下能与氢气或氧气反应
(5)等物质的量的A、B、C三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是_____(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
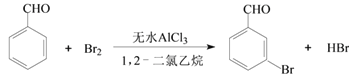
已知:①间溴苯甲醛温度过高时易被氧化。②溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点及相对分子质量见下表:
物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
沸点/℃ | 58.8 | 179 | 83.5 | 229 |
相对分子质量 | 160 | 106 | 185 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
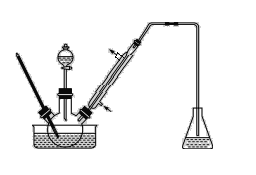
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4nH2O晶体。
步骤4:分离有机层,收集相应馏分。
(1)实验装置中盛装液溴的仪器名称是_____,锥形瓶中的试剂为NaOH溶液其作用为________。
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)___。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3)步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的___(填化学式)。
(4)步骤4中采用何种蒸馏方式_______,其目的是为了防止________。
(5)若实验中加入了5.3 g苯甲醛,得到3.7 g间溴苯甲醛。则间溴苯甲醛产率为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com