
【题目】标准状况下V L氨气溶解在1L水中(水的密度近似为1g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为ω,物质的量浓度为c mol·L-1,则下列关系中不正确的是( )
A. ω=![]() B. ω=
B. ω=![]()
C. ρ=![]() D. c=
D. c=![]()
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
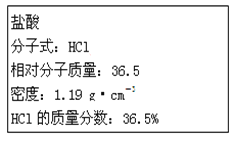
(1)该浓盐酸中HCl的物质的量浓度为____mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是___
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液的密度 D.溶液中Cl-的数目
(3)下列容量瓶的使用方法中,不正确的是____
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至离刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至离刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.200 mol·L-1的稀盐酸。
①所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外还需_____。
②该学生需要用量筒量取___mL上述浓盐酸进行配制。在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏大的有____
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.用量筒量取浓盐酸时俯视观察凹液面
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。

(1)步骤1的主要操作是___________。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)__________,固体残渣的成分是(填化学式)________________。
(3)步骤3中涉及的操作是:蒸发浓缩、_____________、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应温度 |
A | 0.1mol Mg | 6mol/L硝酸 | 10mL | 30℃ |
B | 0.1mol Mg | 3mol/L盐酸 | 10mL | 60℃ |
C | 0.1mol Fe | 3mol/L盐酸 | 10mL | 60℃ |
D | 0.1mol Mg | 3mol/L盐酸 | 10mL | 30℃ |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 离子,分别取样,
离子,分别取样,![]() 测得溶液显弱碱性;
测得溶液显弱碱性;![]() 加入足量盐酸,有无色无味气体产生。为确定溶液组成,还需要检测的离子是
加入足量盐酸,有无色无味气体产生。为确定溶液组成,还需要检测的离子是![]()
![]()
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知固体Na2SO3受热分解生成两种正盐,实验流程和结果如下:
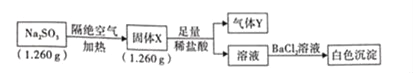
已知:气体Y是一种纯净物,在标准状况下密度为1.518gL﹣1.请回答下列问题:
(1)气体Y的电子式为_____。
(2)实验流程中,Na2SO3受热分解的化学方程式为_____。
(3)另取固体X试样和Na2SO3混合,加适量蒸馏水溶解,再加入稀盐酸,立即有淡黄色沉淀产生。则产生淡黄色沉淀的离子方程式为_____(不考虑空气的影响)。
(4)Na2SO3长期露置在空气中,会被氧化成Na2SO4,检验Na2SO3是否变质的实验操作是_____。
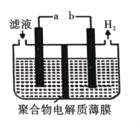
(5)某研究性学习小组通过图所示装置,利用电化学方法处理上述流程中产生的气体Y.基本工艺是将气体Y通入FeCl3,待充分反应后过滤,将所得滤液加入电解槽中进行电解,电解后的滤液可以循环利用。则与a相连的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。下列说法错误的是
A.Na3N是由离子键形成的离子化合物
B.Na3N与盐酸反应生成两种盐
C.Na3N与水的反应属于氧化还原反应
D.Na3N中两种粒子的半径:r(Na+)>r(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病的药物。以2氯苯甲醛为原料合成该药物的路线如下:

(1)A中官能团名称为___________。
(2)C生成D的反应类型为___________。
(3)X( C6H7BrS)的结构简式为____________________________。
(4)写出C聚合成高分子化合物的化学反应方程式:______________________________。
(5)物质G是物质A的同系物,比A多一个碳原子,符合以下条件的G的同分异构体共有___________种。
①除苯环之外无其他环状结构;②能发生银镜反应。
其中核磁共振氢谱中有5个吸收峰,且峰值比为2︰2︰1︰1︰1的结构简式为___________。
(6)已知: 。写出以乙烯、甲醇为有机原料制备化合物
。写出以乙烯、甲醇为有机原料制备化合物![]() 的合成路线(无机物任选)_____________。
的合成路线(无机物任选)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题。

(1)该浓盐酸中HCl的物质的量浓度为__________molL﹣1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_________。
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl﹣的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次,并在操作步骤空白处填上适当仪器名称)_________。
A.用30 mL水洗涤__2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用__加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”,填B表示“偏小”,填C表示“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面__;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com