
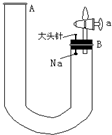
 如图是有关钠与水反应及产物验证的改进实验装置.实验开始时先向管内加入滴有酚酞的水,使水位至B端管口,如图所示,迅速塞紧橡胶塞(此时活塞a是关闭的),使钠块掉入水中.回答下列问题:
如图是有关钠与水反应及产物验证的改进实验装置.实验开始时先向管内加入滴有酚酞的水,使水位至B端管口,如图所示,迅速塞紧橡胶塞(此时活塞a是关闭的),使钠块掉入水中.回答下列问题:

 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
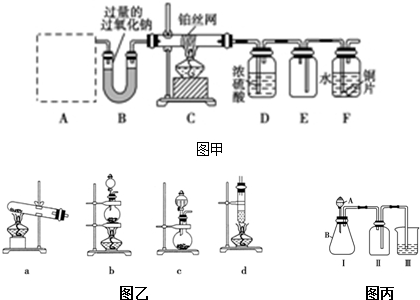
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
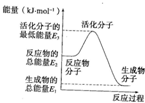 已知:①H2O(g)═H2O(l)△H2=-44kJ?mol-1
已知:①H2O(g)═H2O(l)△H2=-44kJ?mol-1| A、反应②中的能量变化如图所示,则△H2=E1-E3 |
| B、H2的燃烧热为△H=-241.8kJ?mol-1 |
| C、由反应③知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为92.4kJ |
| D、反应③中加入催化剂,通过降低反应所需的活化能来增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、e和f组成的化合物可吸收宇航员在宇宙飞船活动舱内产生的由d和f组成的气体 |
| B、活动舱内还要营造一种适合宇航员生存的人工生态环境,即充入a和f的常见单质 |
| C、c和f以原子个数之比为1:1组成的化合物可用作宇航员所需f单质的来源 |
| D、若潘多拉星球上存在b,地球上此元素主要以b形式存在,b比b少一个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
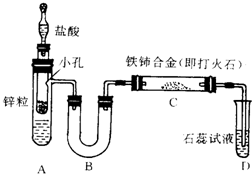 已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.
已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


 、
、 和
和 ,它们的物质的量之比为
,它们的物质的量之比为 (用反应流程图表示并注明反应条件)
(用反应流程图表示并注明反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液操作时,若要回收上层液体,应先从上口倒出上层液体,再从下口将下层液体放出 |
| B、浓的NaOH溶液不慎溅到皮肤上,可无用大量水冲洗,再涂上硼酸或稀醋酸溶液 |
| C、AlCl3溶液中加入过量NaF固体,再滴加氨水,无沉淀产生说明[AlF6]3-很难电离 |
| D、检验Cl-时,为了排除SO42-的干扰,可先滴加过量的Ba(NO3)2溶液后,取上层溶液,再滴加AgNO3溶液,若有白色沉淀,则表明原溶液中有Cl-存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com