
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

①中试剂 | ①中现象 | 解释 | |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | 酸性Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成BaSO3沉淀 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
A. ①②④ B. ①④⑥ C. ②③⑤ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中只含有共价键的是 ( )
A. NaCl、HCl、H2O、NaOHB. Cl2、Na2S、HCl、SO2
C. HBr、CO2、H2O、CS2D. Na2O2、H2O2、H2O、O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生产或实验事实得出的相应结论不正确的是
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | A、B两支试管,各加入4mL0.01mol/L的KMnO4酸性溶液,在A试管中加入2mL0.01mol/LH2C2O4溶液和在B试管中加入4mL 0.02mol/L的H2C2O4溶液,记录溶液褪色所需时间,B试管褪色时间短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物NO3是常见的大气污染物,化学上采用NH3处理NxOy不仅可以消除污染,还可作为工业生产的能量来源。
(1)已知:I.2NO(g)=N2(g)+O2(g) △H=-177kJ/mol
II.4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1253.4kJ/mol
则用NH3处理NO生成氮气和气态水的热化学方程式为__________________。
(2)已知:N2(g)+3H2(g) ![]() 2NH3(g)△H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
2NH3(g)△H<0。不同温度下,向三个一样的容器中投入相同的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。

①M点的v正_________Q点的v正(填“>”“<”或“=”),原因是________________________。
②维持10MPa、T3℃的条件不变,要提高H2的转化率,可以采取的措施是__________________(任写一条)。
③图中三条曲线对应的温度T1、T2、T3由高到低的顺序为__________________。
④恒温恒容条件下,能说明反应N2(g)+3H2(g) ![]() 2NH3(g)达到平衡状态的是_________(填选项字母)
2NH3(g)达到平衡状态的是_________(填选项字母)
A.c2(NH3)/[c(N2 )c3(H2)]保持不变
B.3mol H-H键断裂的同时,有2mol N-H键断裂
C.2v(N2)=v(NH3)
D.反应器中的压强不再发生变化
⑤T3温度下,将1molN2和3molH2充入2L的密闭容器中,维持压强为60MPa不变,达到N点的平衡状态,反应的浓度平衡常数Kc=_____________ (mol/L)-2(用最简分数表示),M点的平衡常数比N点的平衡常数_________(填“大”“小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,向A和B中都充人2molX和2molY,起始VA=0.8a L,VB=a L保持温度不变,在有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
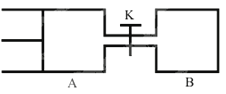
A. 两容器中达到平衡的时间A<B
B. 打开K达到新平衡后,升高B容器温度,A容器体积相比原平衡状态时一定增大
C. A容器中X的转化率为25%,且比B容器中的X的转化率小
D. 打开K一段时间达平衡时,A的体积为0.8a L(连通管中的气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
①N2O4的消耗速率与NO2的生成速率之比为1∶2;②NO2的生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧
C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com