
【题目】分析下图所示的四个原电池装置,其中结论正确的是( )
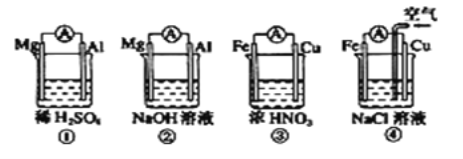
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为2H2O+2e-=2OH-+H2↑
C.③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D.④中Cu作正极,电极反应式为2H++2e-=H2↑
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某有机物由C、H、O三种元素组成。取8.88g样品在如下装置中用电炉加热充分燃烧,通过测定生成的CO2和H2O的质量,再借助质谱图确定其分子式。
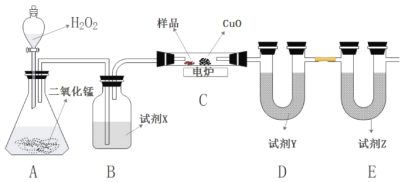
请回答下列问题:
(1)B装置中试剂X为____________。
(2)D装置中试剂Y为_______(填“无水氯化钙”或“碱石灰”下同),E装置中试剂Z为_________。
(3)如果C装置中没有CuO,碱石灰装置的增重将____________(填“增大”“减”或“不变”下同)。
(4)实验测得无水氯化钙装置增重10.8g;碱石灰裝置增重21.12g,由质谱仪测得该有机物的相对分子量为74,则该有机物的分子式为___。
(5)该有机物红外光谱图上有羟基的强吸收峰,试写出该有机物可能的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当用酸滴定碱时,下列操作中会使测定结果(碱的浓度)偏低的是
A.酸式滴定管滴至终点后,俯视读数
B.碱液移入锥形瓶后,加了10 mL蒸馏水再滴定
C.酸式滴定管用蒸馏水润洗后,未用标准液润洗
D.酸式滴定管注入酸液后,尖嘴留有气泡即开始滴定,滴定终点时气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌化妆品的主要成分Z具有美白功效,原从杨树中提取,现可用如图所示反应合成。下列对X、Y、Z的叙述,正确的是( )

A.X、Y和Z均能和NaOH溶液反应
B.X和Z均能和Na2CO3溶液反应,但不能和NaHCO3溶液反应
C.相同物质的量的X和Z,与足量浓溴水发生反应,消耗Br2的物质的量相同
D.Y分子中所有原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 的 Ksp为
的 Ksp为![]() ,将适量
,将适量![]() 固体溶于100mL水中至刚好饱和,该过程中
固体溶于100mL水中至刚好饱和,该过程中![]() 和
和![]() 浓度随时间变化关系如图
浓度随时间变化关系如图![]() 饱和
饱和![]() 溶液中 c(Ag+)=0.034mol/L)。若 t
溶液中 c(Ag+)=0.034mol/L)。若 t![]() 时刻在上述体系中加入100mL0.020mol/L的Na2SO4溶液,下列示意图中,能正确表示 t
时刻在上述体系中加入100mL0.020mol/L的Na2SO4溶液,下列示意图中,能正确表示 t![]() 时刻后
时刻后![]() 和
和![]() 浓度随时间变化关系的是
浓度随时间变化关系的是![]()
![]()
A.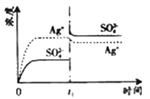 B.
B.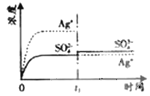
C.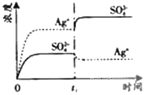 D.
D.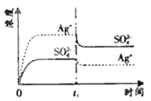
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N、Cu及其相关化合物用途非常广泛。回答下列问题:
(1)基态铜原子的价电子排布式为__________________。
(2)铜与钾处于同周期且最外层电子数相同,铜的熔沸点及硬度均比钾大,其原因是___________________________。
(3)NH3分子的立体构型为_________,中心原子的杂化类型是_________。
(4)N、S、P是组成蛋白质的常见元素。三种元素中第一电离能最大的是_________,电负性最小的是_________。(填元素符号)
(5)已知:Cu2O熔点为1235℃,CuCl熔点为426℃,则可判定Cu2O为_________ (填“离子晶体”或“分子晶体”,下同),CuCl为_________。
(6)氮与铜形成的一种化合物的晶胞结构如图所示。
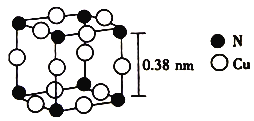
与每个Cu原子紧邻的Cu原子有_________个,阿伏加德罗常数的数值为NA,该晶体的密度为_________ (列出计算式)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是

A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取无水氯化镁的装置图,下列有关表述正确的是
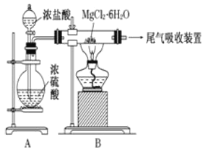
A.装置A中圆底烧瓶中可以换成固体MnO2
B.如果直接加热MgCl26H2O不能得到无水氯化镁,将得到Mg(OH)Cl或MgO
C.尾气吸收可以用浓硫酸作为吸收剂进行吸收
D.金属镁在空气中燃烧,剧烈反应生成氧化镁,如果金属镁燃烧发生火灾,要立即用二氧化碳灭火器进行灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径获得热量:
途径Ⅰ:C(s)+O2(g)═CO2(g) △H1<0 ①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)═CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)═2CO2(g) △H3<0 ③
2H2(g)+O2(g)═2H2O(g) △H4<0 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上____(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
(2)途径Ⅱ在制水煤气的反应里,反应物所具有的总能量____生成物所具有的总能量(填“大于”、“等于”或“小于”),因此在反应时,反应物就需要___能量才能转化为生成物。
(3)途径I中通常将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是______
①使煤充分燃烧,提高能量的转化率 ②减少SO2的产生,避免造成“酸雨”
③减少有毒的CO产生,避免污染空气 ④减少CO2的产生,避免“温室效应”
(4)△H1、△H2、△H3、△H4的数学关系式是____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com