
����Ŀ��������ͼ��ʾװ�ý���ʵ�飬��ش��������⣺

��.(1)��ͨ��SO2���壬����д���пո�
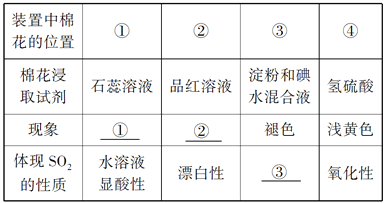
��________________ ��________________ ��________________
(2)д�����з�Ӧ�����ӷ���ʽ��__________________________��
��.��ͨ��HCl���壬װ���е��Ĵ��������������´������ٰ�����ˮ��ʪ��ij�������ʣ��ڽ���KI��Һ���۽���ʯ����Һ���ܽ���ŨNaOH��Һ����ش�
(1)�۲쵽�ڴ����ػ�ɫ���ʲ������ٴ����е�ij�������ʿ��������е�________(�����)���䷴Ӧ�����ӷ���ʽΪ________________________��
a��MnO2 b��KMnO4 c��KCl d��Cu
(2)ʵ������У��ڢ۴��ܹ۲쵽___________________________��
(3) ʵ����һ���ö���������Ũ���ᷴӦ��ȡ������������7.1gCl2ʱ����������HCl�����ʵ���Ϊ_____��
���𰸡� ��� ��ɫ ��ԭ�� I2��SO2��2H2O===SO42-��4H����2I�� b 2MnO4-��10Cl����16H��===2Mn2����5Cl2����8H2O �ȱ�����ɫ 0.2mol
��������I����1���ٶ��������ܺ�ˮ��Ӧ���������ᣬ�������ܵ����������ʹ��Һ�����ԣ�ʯ����Һ������ɫ���ڶ���������Ư���ԣ���ʹƷ����Һ��ɫ�� �۶��������л�ԭ�ԣ����������ԣ���������͵��ܷ���������ԭ��Ӧ��ʹ���ۺ͵�ˮ���Һ��ɫ����2�����������ܺ͵ⷢ��������ԭ��Ӧ�������������ᣬ���ӷ���ʽΪI2+SO2+2H2O=SO42-+4H++2I-��
��1���Ȼ���͵⻯�ز���Ӧ�����Ȼ����л�ԭ�ԣ��ܱ�ǿ������������������������Ӧѡȡǿ���������ܰ��Ȼ�������������������ǿ�����Ե�����ֻ�и�����أ���ѡb�����������ӷ���ʽΪ2MnO4-��10Cl����16H����2Mn2����5Cl2����8H2O����2��������ˮ��Ӧ��������ʹ����ᣬ������Һ�����ԣ�ʯ����Һ�����Ժ�ɫ����������Ư���ԣ���ʹ��Һ��ɫ�����Կ������������ȱ�����ɫ����3��7.1g���������ʵ�����7.1g��71g/mol��0.1mol���������ԭ���غ��֪���������Ȼ�����0.2mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����
A. ţ���Ǵ�����������ڸ߷��ӻ�����
B. ţ���Ǹ�֬����ĸ�����
C. ţ�Ϳ����ڼ��������¼���ˮ��
D. ��ҵ�Ͽɽ�ţ�ͼ����Ƴ�Ӳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������������(����������������)������������Ʒ�Ĺ�ҵ�������£�
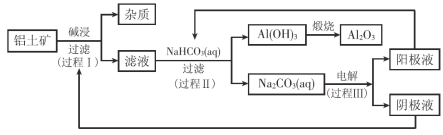
��1������I��������Ӧ�����ӷ���ʽ�� ��
��2������II����һ��Ũ�ȵ�NaHCO3��Һ�����������Һ��������ҺpH��Al(OH)3���ɵ��������NaHCO3��Һ����仯���������£�
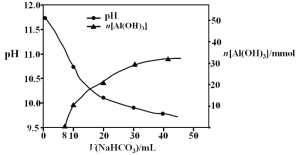
�� ����NaHCO3��Һ���С��8 mLʱ��������Ҫ��Ӧ�����ӷ���ʽ�� ��
�� ����II����Al(OH)3�����ӷ���ʽ�� ��
��3������III�����Na2CO3��Һ��װ������ͼ��ʾ��
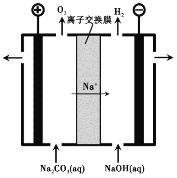
�� �����ĵ缫��Ӧʽ�� ��
�� ��������Һ���ɵ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ����������������¹ʣ��貦�ȵ绰�����ȵ绰�ĺ���Ϊ��
A. 10086 B. 10010 C. 95518 D. 120
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и��������б�ֵΪ2:1����
A������NaHSO4���������������������֮��
B��0.2mol��L��1��CH3COOH��Һ��0.1mol��L��1��������c��H����֮��
C��pH��7�İ�ˮ����NH4��2SO4�Ļ����Һ����c��NH![]() ����c��SO
����c��SO![]() ��֮��
��֮��
D��pH��12��Ba��OH��2��Һ��pH��12��KOH��Һ��c��OH����֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ѧʵ��С��Ϊ��֤���ͱȽ�SO2����ˮ�����ʣ����������װ�ã�
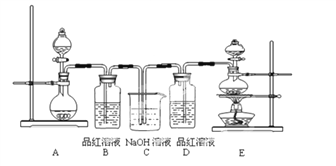
��1��ʵ���ҳ���װ��E�Ʊ�Cl2����Ӧ��Ũ���������ֳ���������__________��
��2����Ӧ��ʼ����B��D���������е�Ʒ����Һ����ɫ��ֹͣͨ����B��D���ȣ�B�е�����Ϊ��_____________________��
��3��װ��C��������_____________________��
��4����ʵ��С��ļס�����λͬѧ��������������װ�ð���ͼװ�ü�������ʵ�飺
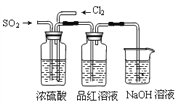 ͨ��һ��ʱ���ͬѧʵ�������Ʒ����Һ��������ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz���Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
ͨ��һ��ʱ���ͬѧʵ�������Ʒ����Һ��������ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz���Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
���Է�����ͬѧʵ������У�Ʒ����Һ����ɫ��ԭ���ǣ��÷���ʽ��ʾ����_____________��
������Ϊ��ͬѧ������������Ʒ����Һ���Խ��Խdz�ģ�____________________��
��5��������������������꣬������ˮ��Ʒ1�ݣ�ÿ��һ��ʱ��ⶨ����ˮ��Ʒ��pH�������������±���
����ʱ��/h | 0 | 1 | 2 | 3 | 4 |
��ˮ��pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
�������ݣ��ش��������⣺
����ˮ��Ʒ��pH�仯��ԭ���ǣ��û�ѧ��Ӧ����ʽ��ʾ��_____________��
������Ϊ�������������;���ɲ��õĴ�ʩ��________��
A.����ú��ȼ�ϡ� B.�ѹ����̴����
C.ȼ������ D.�����ữ�������м�ʯ�ҡ�E.��������Դ
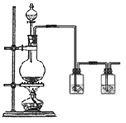
(6)ʵ������Ҫ�ø��﴿��������������װ��ͼ��һ��ϴ��ƿ��ʢ�ŵ�Һ��Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.2 molL-1��һԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ������˵����ȷ����
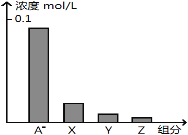
A��HAΪǿ��
B���û��ҺpH=7
C��ͼ��X��ʾHA��Y��ʾOH-��Z��ʾH+
D���û����Һ�У�c(A-)+c(Y)=c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥMgCl2��Һ�е�FeCl3�����ڼ��Ƚ��������������һ���Լ��������Լ���
A��NaOH B����ˮ C��Na2CO3 D��MgO
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com