
【题目】常温下,下列各组数据中比值为2:1的是
A.熔融NaHSO4电离出的阳离子与阴离子之比
B.0.2mol·L-1的CH3COOH溶液与0.1mol·L-1的盐酸中c(H+)之比
C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH![]() )与c(SO
)与c(SO![]() )之比
)之比
D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中c(OH-)之比
【答案】C
【解析】
试题分析:A、熔融NaHSO4电离出的阳离子与阴离子之比为1:1,故A错误;B、CH3COOH为弱电解质,不能完全电离,0.2molL-1的CH3COOH溶液与0.1molL-1的盐酸中c(H+)之比小于2:1,故B错误;C、溶液呈电中性,则有c(NH4+)+c(H+)=2c(SO42-)+c(OH-),pH=7,则c(H+)=c(OH-),所以c(NH4+)与c(SO42-)之比为2:1,故C正确;D、pH=12的Ba(OH)2溶液中c(Ba(OH)2)=![]() ×c(OH-)=0.005mol/L,pH=12的KOH溶液中c(KOH)=c(OH-)=0.01mol/L,二者比值为1:2,故D错误;故选C。
×c(OH-)=0.005mol/L,pH=12的KOH溶液中c(KOH)=c(OH-)=0.01mol/L,二者比值为1:2,故D错误;故选C。


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】已知卤代烃可以和钠发生反应.例如溴乙烷与钠发生反应为2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列所给化合物中与钠反应不可能生成环丁烷的是 ( )
A. CH3CH2CH2CH2Br B. CH2BrCH2Br
C. CH2Br2 D. CH2BrCH2CH2CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:
操作 | 现象 |
取一块打磨过的生铁片,在其表面滴1滴含酚酞和K3[Fe(CN)6]的食盐水 |
放置一段时间后,生铁片上出现如右图所示“斑痕”。其边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈 |
下列说法不合理的是
A. 生铁片发生吸氧腐蚀
B. 中心区:Fe–2e—==Fe2+
C. 边缘处:O2+2H2O+4e—==4OH—
D. 交界处:4Fe2++O2+10H2O==4Fe(OH)3+8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO3- ⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是
A.①③⑤⑦⑧ B.②④⑦ C.①⑥ D.②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
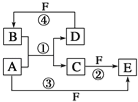
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 ,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是 ,已知光照条件下D与F方可以反应.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 .将标准状况下3.36L 物质E 与10.0g 氢氧化钠溶液充分反应,所得溶液溶质成分为 (写出化学式和对应的物质的量).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如下图所示装置进行实验,请回答下列问题:

Ⅰ.(1)若通入SO2气体,请填写表中空格:
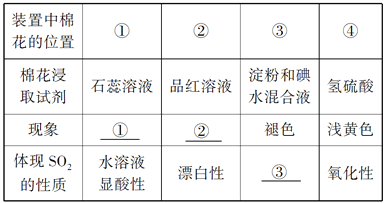
①________________ ②________________ ③________________
(2)写出③中反应的离子方程式:__________________________。
Ⅱ.若通入HCl气体,装置中的四处棉花依次做了如下处理:①包有用水润湿的某固体物质;②浸有KI溶液;③浸有石蕊溶液;④浸有浓NaOH溶液。请回答:
(1)观察到②处有棕黄色物质产生,则:①处包有的某固体物质可能是下列的________(填序号),其反应的离子方程式为________________________。
a.MnO2 b.KMnO4 c.KCl d.Cu
(2)实验过程中,在③处能观察到___________________________。
(3) 实验室一般用二氧化锰与浓盐酸反应制取氯气,当生成7.1gCl2时,被氧化的HCl的物质的量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84.回答下列问题:
(1)烃A的分子式为 。
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是 ;若总质量一定,充分燃烧消耗氧气的量不变的是 。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(3)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。
① A的结构简式为 名称为 。
② 链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式: 。
③ 与A互为同分异构体,且主链碳原子个数与A相同的链烃有 种(不包括A)
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com