
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
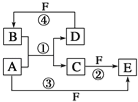
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 ,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是 ,已知光照条件下D与F方可以反应.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 .将标准状况下3.36L 物质E 与10.0g 氢氧化钠溶液充分反应,所得溶液溶质成分为 (写出化学式和对应的物质的量).
【答案】(1)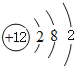 ;C+4HNO3(浓)
;C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)2Fe2++Cl2═2Fe3++2Cl﹣;
(3)2C+SiO2![]() Si+2CO↑;Na2CO2,0.1mol;NaHCO3,0.05mol.
Si+2CO↑;Na2CO2,0.1mol;NaHCO3,0.05mol.
【解析】试题分析:(1)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,A最外层电子数小于4且为偶数,D位于第二周期、A位于第三周期,则A是Mg、D是C元素;F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2;
(2)若A是常见的变价金属的单质,D、F是气态单质,A是Fe,反应①、反应②都在在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2;
(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则A为C,D为Si,F为O2,B为SiO2,反应①为C与二氧化硅的反应,C是CO,E为CO2.
解:(1)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,A最外层电子数小于4且为偶数,D位于第二周期、A位于第三周期,则A是Mg、D是C元素;F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2.
则A的原子结构示意图为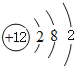 ,反应④的化学方程式为:C+4HNO3(浓)
,反应④的化学方程式为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,
CO2↑+4NO2↑+2H2O,
故答案为: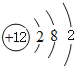 ;C+4HNO3(浓)
;C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)若A是常见的变价金属的单质,D、F是气态单质,A是Fe,反应①、反应②都在在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2.反应②在水溶液中进行反应,其离子方程式是:2Fe2++Cl2═2Fe3++2Cl﹣,
故答案为:2Fe2++Cl2═2Fe3++2Cl﹣;
(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则A为C,D为Si,F为O2,B为SiO2,C是CO,E为CO2.反应①为C与二氧化硅的反应,反应方程式为:2C+SiO2![]() Si+2CO↑,
Si+2CO↑,
将标准状况下3.36L二氧化碳为![]() =0.15mol,10.0g 氢氧化钠为
=0.15mol,10.0g 氢氧化钠为![]() =0.25mol,二者物质的量之比为3:5,介于2:1与1:1之间,则生成Na2CO3、NaHCO3,设二者物质的量分别为xmol、ymol,则
=0.25mol,二者物质的量之比为3:5,介于2:1与1:1之间,则生成Na2CO3、NaHCO3,设二者物质的量分别为xmol、ymol,则![]() ,解得x=0.1,y=0.05,
,解得x=0.1,y=0.05,
故答案为:2C+SiO2![]() Si+2CO↑;Na2CO2,0.1mol;NaHCO3,0.05mol.
Si+2CO↑;Na2CO2,0.1mol;NaHCO3,0.05mol.


科目:高中化学 来源: 题型:
【题目】如下图所示为4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假设碳原子上其余的化学键都与氢原子结合。

(1)图中属于烷烃的是_____________(填字母,下同)。
(2)在如上图所示的有机化合物中,碳原子与碳原子之间不仅可以形成单键,还可以形成_____________和_____________;不仅可以形成_____________,还可以形成碳环。
(3)含有双键的是_____________,含有三键的是_____________。
(4)图中互为同分异构体的是:A与________;B与________;D与________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年我国科研人员研制出一种室温“可呼吸”NaCO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是:

A.“吸入”CO2时,钠箔为正极
B.“呼出”CO2时,Na+向多壁碳纳米管电极移动
C.“吸入”CO2时的正极反应:4Na+ + 3CO2 + 4e—= 2Na2CO3 + C
D.标准状况下,每“呼出”22.4LCO2,转移电子数为0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3:PbSO4(s) + CO32—(aq) ![]() PbCO3(s) + SO42—(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是
PbCO3(s) + SO42—(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是
A. PbSO4的溶解度小于PbCO3
B. 处理PbSO4后,Na2CO3或NaHCO3溶液的pH升高
C. 若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大
D. 整个过程涉及一个复分解反应和两个氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组数据中比值为2:1的是
A.熔融NaHSO4电离出的阳离子与阴离子之比
B.0.2mol·L-1的CH3COOH溶液与0.1mol·L-1的盐酸中c(H+)之比
C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH![]() )与c(SO
)与c(SO![]() )之比
)之比
D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中c(OH-)之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列污水处理的方法中,表示其原理的离子方程式不正确的是
A.混凝法,用明矾做混凝剂:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
B.中和法,用过量CO2中和碱性废水:CO2+2OH—=CO32—
C.沉淀法,用Na2S处理含Hg2+废水:Hg2++S2—=HgS↓
D.氧化还原法,用FeSO4将酸性废水中Cr2O72—还原为Cr3+:Cr2O72—+6Fe2++14H+=2Cr3++6Fe3++7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 该温度下此反应的平衡常数K =1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com