
【题目】下列过程中,需要增大化学反应速率的是( )
A.钢铁腐蚀
B.食物腐败
C.塑料老化
D.工业合成氨
科目:高中化学 来源: 题型:
【题目】85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得年诺贝尔生理学或医学奖,颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图),下列说法错误的是
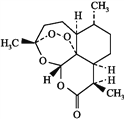

青蒿素 双氢青蒿素
A. 青蒿素和双氢青蒿素互为同分异构体
B. 由青蒿素制备双氢青蒿素的反应属还原反应
C. 青蒿素的分子式为C15H22O5
D. 青蒿素分子中含有过氧键和酯基、醚键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
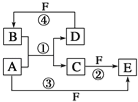
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 ,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是 ,已知光照条件下D与F方可以反应.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 .将标准状况下3.36L 物质E 与10.0g 氢氧化钠溶液充分反应,所得溶液溶质成分为 (写出化学式和对应的物质的量).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84.回答下列问题:
(1)烃A的分子式为 。
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是 ;若总质量一定,充分燃烧消耗氧气的量不变的是 。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(3)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。
① A的结构简式为 名称为 。
② 链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式: 。
③ 与A互为同分异构体,且主链碳原子个数与A相同的链烃有 种(不包括A)
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol苯乙烯(![]() )中含有的C=C数为4NA
)中含有的C=C数为4NA
B.标准状况下,2.24L己烷含有的分子数为0.1NA
C.1mol甲基含10NA个电子
D.某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是
A.H+、 Na+、HCO3-、Cl- B.Cu2+、Na+、 Cl-、、SO42-
C.Mg2+、K+、SO42-、OH- D.Ag+、Al3+、NO3- 、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列物质与NaOH溶液、稀H2SO4、H2O2溶液均能发生反应的是
A. Fe(NO3)2 B. SiO2 C. Al(OH)3 D. CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
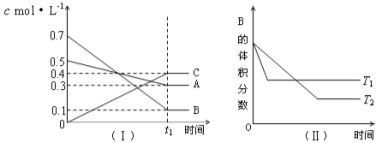
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.在(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动
C.T℃时,在相同容器中,若由0.3mol·L—1 A 、0.1 mol·L—1 B和0.4 mol·L—1 C反应,达到平衡后,C的浓度仍为0.4 mol·L—1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com