
【题目】如下图所示为4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假设碳原子上其余的化学键都与氢原子结合。

(1)图中属于烷烃的是_____________(填字母,下同)。
(2)在如上图所示的有机化合物中,碳原子与碳原子之间不仅可以形成单键,还可以形成_____________和_____________;不仅可以形成_____________,还可以形成碳环。
(3)含有双键的是_____________,含有三键的是_____________。
(4)图中互为同分异构体的是:A与________;B与________;D与________。
【答案】(1)ACH (2)双键 三键 碳链
(3)BEF DG (4)C E、F、H G
【解析】(1)烷烃中碳原子之间都以单键形式结合,由此可以判断,题中属于烷烃的是A、C和H。(2)观察题中的有机化合物,可以看出碳原子与碳原子之间不仅可以形成单键,还可以形成双键,如B、E、F,也可以形成三键,如D、G;碳原子与碳原子之间不仅可以形成碳链,还可以形成碳环。(3)每个小球表示一个碳原子,每根小棍表示一个单键,可知A的分子式为C4H10;B的分子式为C4H8,分子中存在双键;C的分子式为C4H10;D的分子式为C4H6,分子中存在三键;E的分子式为C4H8;F的分子式为C4H8;G的分子式为C4H6;H的分子式为C4H8,分子中碳原子之间形成碳环。(4)A与C互为同分异构体,B与E、F、H互为同分异构体,D与G互为同分异构体。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);ΔH <0的化学反应下列叙述不正确的是
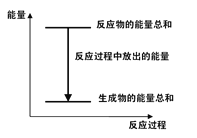
A.反应过程中能量关系可用如图表示
B.若将该反应设计成原电池锌为负极
C.ΔH的值与反应方程式的计量系数无关
D.若将其设计为原电池当有32.5g锌溶解时,正极放出气体一定为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是电解饱和氯化钠溶液示意图。图2中,x轴表示实验时流入阴极的电子的物质的量,y轴表示
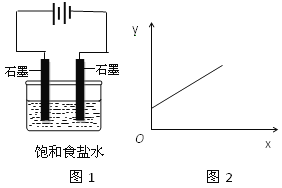
A.n(Na+) B.n(Cl-)
C.c(OH-) D.c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。大多数+1价铜的化合物是难溶物,如:Cu2O、CuI、CuCl、CuH等。
(1)在新制Cu(OH)2悬浊液中滴入葡萄糖溶液,加热生成不溶物的颜色为: ,某同学实验时却有黑色物质出现,这种黑色物质的化学式为: 。
(2)在CuCl2溶液中逐滴加入过量KI溶液可能发生:
a.2Cu2++4I- =2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I- =2CuCl↓(白色)+I2。
为顺利观察到白色沉淀可以加入的最佳试剂是 。
A.SO2 B.苯 C.NaOH溶液 D.乙醇
(3)一定条件下,在CuSO4中加入NH5反应生成氢化亚铜(CuH)。
①已知NH5是离子晶体且所有原子都达到稀有气体的稳定结构,请写出NH5的电子式: 。
②写出CuH在过量稀盐酸中有气体生成的离子方程式 。
③将CuH溶解在适量的稀硝酸中, 完成下列化学方程式
![]()
(4)常温下,向0.20 mol L-1硫酸铜溶液中加入氢氧化钠溶液,生成浅蓝色氢氧化铜沉淀,当溶液的pH = 6时,c(Cu2+)=________________mol.L1。
[已知:![]()
![]() ]
]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是
A. 4 s时c(B)为0.38 mol/L
B. 830℃达平衡时,A的转化率为20%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为0.4
A(g)+B(g)的平衡常数为0.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知卤代烃可以和钠发生反应.例如溴乙烷与钠发生反应为2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列所给化合物中与钠反应不可能生成环丁烷的是 ( )
A. CH3CH2CH2CH2Br B. CH2BrCH2Br
C. CH2Br2 D. CH2BrCH2CH2CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得年诺贝尔生理学或医学奖,颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图),下列说法错误的是
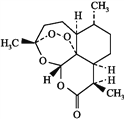

青蒿素 双氢青蒿素
A. 青蒿素和双氢青蒿素互为同分异构体
B. 由青蒿素制备双氢青蒿素的反应属还原反应
C. 青蒿素的分子式为C15H22O5
D. 青蒿素分子中含有过氧键和酯基、醚键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
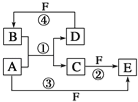
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 ,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是 ,已知光照条件下D与F方可以反应.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 .将标准状况下3.36L 物质E 与10.0g 氢氧化钠溶液充分反应,所得溶液溶质成分为 (写出化学式和对应的物质的量).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com