
【题目】水芹烯是一种具有祛痰、抗菌、杀虫作用的添加剂,由水芹烯合成聚合物 H 的路线如图所示。
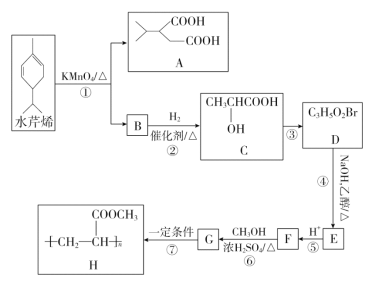
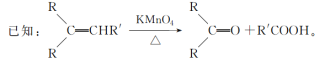
回答下列问题:
(1)B 的结构简式为________,G 的结构简式是________。
(2)反应③的反应试剂和反应条件分别是________,反应④的反应类型是________。
(3)反应⑥的化学方程式为________,反应⑥中浓 H2SO4 的作用是________。
【答案】![]() CH2=CHCOOCH3 浓氢溴酸、加热 消去反应 CH2=CHCOOH+CH3OH
CH2=CHCOOCH3 浓氢溴酸、加热 消去反应 CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O 作催化剂和吸水剂
CH2=CHCOOCH3+H2O 作催化剂和吸水剂
【解析】
由题给信息及水芹烯、A的结构简式,可确定B为![]() ;反应②中,
;反应②中,![]() 发生还原反应生成C(
发生还原反应生成C(![]() );反应③中,C发生取代反应生成D(
);反应③中,C发生取代反应生成D(![]() );反应④中,D发生消去反应生成E(CH2=CHCOONa);反应⑤中E与H+反应生成F(CH2=CHCOOH);反应⑥中F与CH3OH发生酯化反应生成G(CH2=CHCOOCH3);反应⑦中G发生加聚反应生成H(
);反应④中,D发生消去反应生成E(CH2=CHCOONa);反应⑤中E与H+反应生成F(CH2=CHCOOH);反应⑥中F与CH3OH发生酯化反应生成G(CH2=CHCOOCH3);反应⑦中G发生加聚反应生成H(![]() )。
)。
(1)由以上分析知,B 的结构简式为![]() ,G 的结构简式是CH2=CHCOOCH3。答案为:
,G 的结构简式是CH2=CHCOOCH3。答案为:![]() ;CH2=CHCOOCH3;
;CH2=CHCOOCH3;
(2)反应③为![]() 发生取代反应生成
发生取代反应生成![]() ,则反应试剂和反应条件分别是浓氢溴酸、加热,反应④为
,则反应试剂和反应条件分别是浓氢溴酸、加热,反应④为![]() 生成 CH2=CHCOONa,反应类型是消去反应。答案为:浓氢溴酸、加热;消去反应;
生成 CH2=CHCOONa,反应类型是消去反应。答案为:浓氢溴酸、加热;消去反应;
(3)反应⑥中,CH2=CHCOOH与CH3OH在浓硫酸、加热条件下发生酯化反应,生成CH2=CHCOOCH3和水,化学方程式为CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O,反应⑥中浓 H2SO4 的作用是作催化剂和吸水剂。答案为:CH2=CHCOOH+CH3OH
CH2=CHCOOCH3+H2O,反应⑥中浓 H2SO4 的作用是作催化剂和吸水剂。答案为:CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O;作催化剂和吸水剂。
CH2=CHCOOCH3+H2O;作催化剂和吸水剂。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X、Y的原子最外层电子数之和为14;X与Z同族;W是空气中含量最多的元素;Z的单质为常见气体,其水溶液具有漂白性。下列说法正确的是![]()
A.X的最高正化合价为![]()
B.简单离子的半径:![]()
C.Y的单质与冷、热水均不反应
D.W、Z两元素形成的化合物![]() 为共价化合物
为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.常温下,![]() 溶液的
溶液的![]()
B.工业上电解饱和食盐水时,以石墨为阴极,铁棒为阳极
C.铅蓄电池放电时,正极电极反应为:![]()
D.常温下,在AgCl悬浊液中加入少量NaCl饱和溶液,![]() 减小,
减小,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的二氧化硫气体和二氧化碳气体的比较中,正确的是( )
A.密度比为11∶16B.物质的量比为16∶11
C.体积比为11∶16D.分子个数比为16∶11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 R、T、Q、W 在元素周期表中的相对位置如图所示,其中 T 所处的周期序数与族序数相等下列判断不正确的是

A.最简单气态氢化物的热稳定性:R >Q
B.最高价氧化物对应水化物的酸性:Q< W
C.R 的氧化物是酸性氧化物
D.含 T 的盐溶液可能显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去) 如下所示:
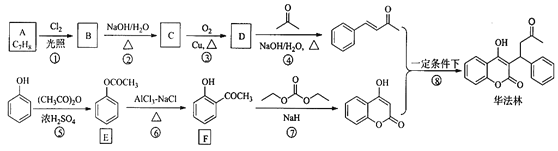
回答下列问题:
(1)A 的名称为________,E 中官能团名称为________。
(2)B 的结构简式为________。
(3)由 C 生成 D 的化学方程式为___________
(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F 的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与 FeCl3 溶液发生显色反应 b.含有-CHO
其中核磁共振氢谱为五组峰的结构简式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)使用甲醇汽油可以减少汽车尾气对环境的污染。工业上在 200℃和 10MPa 的条件下可用甲烷和氧气通过铜制管道反应制得甲醇,已知一定条件下,CH4 和 CH3OH 的燃烧热分别 784kJ/mol 和 628kJ/mol 则 2CH4(g)+O2(g)![]() 2CH3OH(g) △H=_____。
2CH3OH(g) △H=_____。
(2)二甲醚也是清洁能源。用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g) CH3OCH3(g) +H2O(g) △H<0。某温度下,,将 2.0molCO(g)和 6.0molH2(g)充入容积为 2L 的密闭容器中,反应到达平衡时, 改变压强和温度,平衡体系中 CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是_____。
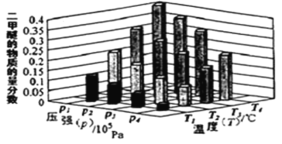
A.p3>p2,T3>T2
B.p1>p3,T1>T3
C.p1>p4,T2>T3
D.p2>p4,T4>T2
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2CO2(g) +N2(g);
2CO2(g) +N2(g);
①200K、pPa时,在一个容积为 2L的恒温密闭容器中充入 1.5molNO 和 2.0molCO,开始反应至 2min 时测得 CO 转化率为 30%,则用N2表示的平均反应速率为v(N2)=_________;反应达到平衡状态时,测得二氧化碳为 0.8mol,则平衡时的压强为起始压强的_________倍(保留两位小数)。
②该反应在低温下能自发进行,该反应的ΔH_____0(填“>”、“<”)
(4)一定温度下,将NO2与SO2以体积比 1:2 置于密闭容器中发生反应NO2(g)+SO2(g) SO3(g)+NO(g),达到平衡时SO3的体积分数为 25%。该反应的平衡常数K= ______。
(5)利用原电池反应可实现NO2 的无害化,总反应为6NO2+ 8NH3=7N2+12H2O,电解质溶液为碱性。工作一段时间后,该电池正极区附近溶液 pH ____(填“变大”、“变小”或“不变”),负极电极反应式为 ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化锰为原料制取高锰酸钾晶体的实验流程如图所示,下列有关说法正确的是
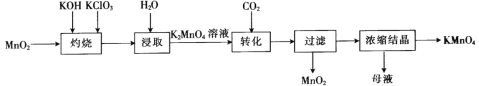
A.“灼烧”时,可在玻璃坩埚中进行
B.“浸取”时,可用无水乙醇代替水
C.“转化”反应中,通入CO2的目的是提供还原剂
D.“浓缩结晶”的目的是分离提纯KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸碱中和滴定是中学化学定量分析的一种重要方法。已知在25℃时,取20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,用浓度为0.1000mol/L的NaOH溶液分别进行滴定,滴定曲线如图所示。下列说法不正确的是( )。

A.在相同温度下,同浓度的三种酸溶液的pH大小顺序为:HZ<HY<HX
B.当V(NaOH)=10mL时,在HY溶液中由水电离出的![]()
C.HY与HZ混合,达到平衡时:![]()
D.根据上述滴定曲线,可计算得Ka(HY)≈10-3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com