
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH的数据如下表所示。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
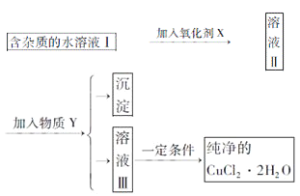
氢氧化物 | 开始沉淀pH | 完全沉淀pH |
Fe(OH)2 | 6.5 | 9.7 |
Fe(OH)3 | 1.5 | 3.7 |
Cu(OH)2 | 4.2 | 6.7 |
请回答下列问题:
(1)本实验最适合的氧化剂X是__________。(选填下面的序号)
A K2Cr2O7 B NaClO C H2O2 D KMnO4
(2)物质Y是________。
(3)本实验用加碱沉淀的目的是否能达到?________________。原因是________________。
(4)除去Fe3+的化学方程式为____________________,_________________________________。
(5)加氧化剂的目的为________________________。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________________。应如何操作________________。
【答案】C CuO或Cu(OH)2 不能 加碱的同时Cu2+也会沉淀下来 Fe3++3H2O ![]() Fe(OH)3+3H+ CuO+2H+= Cu2++H2O 将Fe2+氧化为Fe3+再除去 不能 应在氯化氢气氛中浓缩后冷却结晶
Fe(OH)3+3H+ CuO+2H+= Cu2++H2O 将Fe2+氧化为Fe3+再除去 不能 应在氯化氢气氛中浓缩后冷却结晶
【解析】
本实验的目的是用恰当方法除去CuCl22H2O中的FeCl2,结合已学知识,可想到用沉淀法除去Fe2+,但由题目叙述可知,Fe2+沉淀为氢氧化物时所需pH与Cu2+的沉淀的pH相同,也就是说,Fe2+沉淀的同时,Cu2+也会沉淀,无法将两者分离开.而题目告知Fe3+沉淀所需的pH较小,所以应先将Fe2+氧化为Fe3+后再将其除去;为避免引入新的杂质,结合H2O2还原为H2O的特点,过量时也可用加热的方法使其分解而除去,氧化剂应选用H2O2;为了调节溶液的酸度,使pH在3.7的范围,可用CuO降低溶液中H+浓度,而CuO与酸反应后生成Cu2+,也不引入新的杂质,过量的CuO用过滤的方法与生成的Fe(OH)3沉淀一并除去.CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),所以应在HCl气氛中采用低温减压蒸发结晶的方法,以得到CuCl22H2O的晶体。
(1)进行物质除杂时,所选用的试剂不能引入新的杂质;
A使用重铬酸钾做氧化剂能引入杂质离子,故A错误;
B使用次氯酸钠做氧化剂能引入杂质离子,故B错误;
C.使用双氧水做氧化剂,生成的是水,过量能加热除去,使用氧化铜与酸反应生成的是铜离子,不引入新的杂质,故C正确,
D.使用高锰酸钾做氧化剂能引入杂质离子,故D错误;
答案:C
(2)物质Y是用来调节pH为3.7,使得铁离子完全沉淀,因为不能引入新的杂质,所以用CuO或Cu(OH)2;
答案:CuO或Cu(OH)2
(3)采用加碱法除去氯化亚铁,则铜离子也会沉淀,故不能使用加碱法除去氯化亚铁;
答案: 不能 加碱的同时Cu2+也会沉淀下来
(5)Fe2+沉淀为氢氧化物时所需pH与Cu2+的沉淀的pH相同,也就是说,Fe2+沉淀的同时,Cu2+也会沉淀,无法将两者分离开,根据题干提供信息可知Fe3+沉淀所需的pH较小,所以应先将Fe2+氧化为Fe3+后再将其除去;
答案:将Fe2+氧化为Fe3+再除去
(6)CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),所以应在HCl气氛中采用低温减压蒸发结晶的方法,以得到CuCl22H2O的晶体;
答案:不能 应在氯化氢气氛中浓缩后冷却结晶。


科目:高中化学 来源: 题型:
【题目】已知溶液中存在平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na2CO3溶液,其中固体质量增加
⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
A. ①⑥B. ①⑥⑦C. ②③④⑥D. ①②⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
选项 | A | B | C | D |
实验 | 用CCl4提取溴水中的Br2 | 从食盐水中提取NaCl固体 | 从KI和I2的固体混合物中回收I2 | 配制100 mL 0.100 0 mol·L-1 K2Cr2O7溶液 |
装置或仪器 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A. 1mol甲烷完全燃烧转移的电子数为8NA
B. 18g的D2O中含有的质子数为10NA
C. 28g的乙烯和环己烷混合气体中所含原子总数为6NA
D. 1L1mol/L的NH4C1溶液中NH4+和Cl—的数目均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如下表所示:
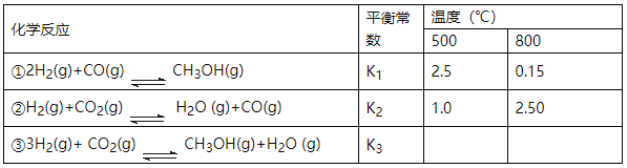
请回答下列问题:
(1)反应②是__________(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示);根据反应③判断△S__________0(填“>”、“=”或“<”),在____________(填“较高”或“较低”)温度下有利于该反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有______________(填写字母序号)。
a.缩小反应容器的容积
b.扩大反应容器的容积
c.升高温度
d.使用合适的催化剂
e.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol·L-1、0.8mol·L-1、0.3mol·L-1、0.15mol·L-1,则此时v正__________v逆(填“>”、“=”或“<”)。
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件随时间的变化曲线,开始时升温,t1时平衡,t2时降压,t3时增加CO浓度,t4时又达到平衡.请画出t2至t4的曲线______。
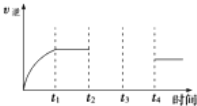
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列9种物质:①氯气;②二氧化硫;③稀硫酸;④铁;⑤BaCl2固体;⑥氢氧化钾;⑦KNO3溶液;⑧酒精(C2H5OH);⑨氧化钙,请将上述物质按要求完成下列问题:
(1)用相应化学式填写下列空白:属于酸性氧化物的有_____________,属于碱性氧化物的有____________,属于电解质的是______,属于非电解质的是_______。(用序号填空)
(2)写出NaHCO3电离方程式:______
(3)用双线桥表示Cl2与二氧化硫的反应________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为__,当6.4g铜溶解时转移电子物质的量为___mol;
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式____;
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓ +I3- ②I3-+2S2O32-= S4O62-+ 3I-
反应①中的还原剂为____,现取10.00mL含Cu2+的溶液,加入足量的KI充分反应后,用0.100 mol/L的Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液25.00mL,此溶液中Cu2+的浓度为__mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,非金属元素被还原的是( )
A. MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2OB. H2+CuO
MnCl2+Cl2↑+2H2OB. H2+CuO![]() Cu+H2O
Cu+H2O
C. 2FeCl2+Cl2===2FeCl3D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质变化和分类的说法正确的是( )
A. 胆矾、冰水混合物、四氧化三铁都不是混合物
B. 电解熔融态的Al2O3、12C转化为14C都属于化学变化
C. 葡萄糖溶液和淀粉溶液的本质区别是能否产生丁达尔效应
D. SiO2、NO2、Al2O3都属于酸性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com