
【题目】在水溶液中,下列电离方程式书写错误的是
A.NaHCO3=Na++H++CO32-
B.Ba(OH)2=Ba2++2OH-
C.NaHSO4=Na++H++SO42-
D.BaCl2=Ba2++2Cl-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:

回答下列问题:
(1)二氧化碳分子中的化学键是_________________,物质乙的化学式是______________。
(2)写出反应①的化学方程式__________________________________。
(3)实验室常用纯净碳酸钙与稀盐酸反应制取二氧化碳气体,反应过程中产生二氧化碳的速率V(CO2) 与时间关系如下图:

①由图像分析,化学反应速率最快一段是___________。
②为了增大上述化学反应的反应速率,欲向溶液中加入下列物质,你认为可行的是_________(填写序号)。
A.蒸馏水 B.氯化钠溶液 C.浓盐酸 D.加热
(4)二氧化碳能与氢氧化钠溶液反应,当氢氧化钠过量时反应生成碳酸钠,当氢氧化钠少量时反应生成碳酸氢钠。当二氧化碳与氢氧化钠反成的物质的量比为2:3时,溶液中的溶质是_______________。
(5)从原子结构角度说明氧原子得电子能力强于碳原子:___________________________________。
(6)在一定条件下,工业上也可用CO2合成甲醇(CH3OH),其化学方程式为:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。 将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,t min时测得甲醇的物质的量为c mol。计算0-t min内CO2的反应速率为_________ mol·L-1·s-1。 [X 的反应速率ν(X)=X的物质的量浓度变化/变化需要的时间]
CH3OH(g)+H2O(g)。 将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,t min时测得甲醇的物质的量为c mol。计算0-t min内CO2的反应速率为_________ mol·L-1·s-1。 [X 的反应速率ν(X)=X的物质的量浓度变化/变化需要的时间]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+682.44kJmol﹣1 ,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)═SiCl4(g)△H=﹣657.01kJmol﹣1
③SiCl4(g)+2Mg(s)═2MgCl2(s)+Si(s)△H=﹣625.63kJmol﹣1
(纯硅)
用石英砂生产1.00kg纯硅的总放热为( )
A.2.43×104 kJ
B.2.35×104 kJ
C.2.23×104 kJ
D.2.14×104 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A. 已知工业合成氨的正反应方向放热,所以升温正反应速率降低,逆反应速率升高
B. 实验室用H2O2分解制备O2,加入MnO2后,反应速率明显加快
C. 2SO2+O2![]() 2SO3反应中,SO2的转化率不能达到100%
2SO3反应中,SO2的转化率不能达到100%
D. 实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的反应方程式正确的是( )
A.亚硫酸钠水溶液显碱性:SO32﹣+2H2O?H2SO3+2OH﹣
B.SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32﹣
C.燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2 ![]() 2CaSO4+2CO2
2CaSO4+2CO2
D.浓NaOH溶液处理少量二氧化硫:SO2+OH﹣═HSO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.
(1)Ⅰ.用高锰酸钾和浓盐酸反应制取氯气 a.该小组利用下图装置及试剂制备并收集适量Cl2 , 装置B、C的作用分别是、 . 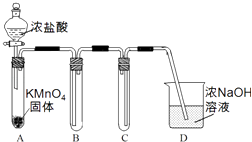
b.制得的氯气中加入适量水,得到饱和氯水,
饱和氯水中含氯元素的微粒有(写出全部微粒).
c.饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一.在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强.
①滤液漂白性增强的原因是(用化学平衡移动原理解释).
②饱和氯水与石灰石反应生成HClO的方程式是 .
(2)ClO3﹣、Cl﹣和H+反应的探究 a.KClO3、KCl与硫酸可以反应.该小组设计了系列实验研究反应条件对反应的影响,实验记录如下(实验在室温下进行):
烧杯编号 | 1 | 2 | 3 | 4 |
氯酸钾饱和溶液 | 1mL | 1mL | 1mL | 1mL |
氯化钾固体 | 1g | 1g | 1g | 1g |
水 | 8mL | 6mL | 3mL | 0mL |
硫酸(6mol/L) | 0mL | 2mL | ()mL | 8mL |
现象 | 无现象 | 溶液呈浅黄色 | 溶液呈黄绿色,生成浅黄绿色气体 | 溶液呈黄绿色, |
①该系列实验的目的 .
②烧杯3取用硫酸的体积应为mL.
b.该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为﹣59℃,液体为红色;Cl2沸点为﹣34℃,液态为黄绿色.设计最简单的实验验证Cl2中含有ClO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25℃时pH=12的NaOH溶液100mL.,欲用以下几种方法将其pH调整到11,回答下列问题(已知混合后溶液的总体积等于混合前两稀溶液的体积之和):
(1)25℃时,pH=12的NaOH溶液中由水电离产生的c(OH﹣)=
(2)加水稀释,需加水的体积为mL.
(3)加入pH=2的盐酸,需加盐酸的体积为mL.(精确到0.1)
(4)加入pH=10的NaOH溶液,需加NaOH溶液的体积为mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:

(1)仪器A的名称是____________。
(2)烧瓶中发生反应的化学方程式为(含条件)________________________。
(3)为在E装置中收集到干燥纯净的氯气,装置C中盛放的试剂为_____________(填写名称),作用是____________________________。
(4)F处盛有Na2S溶液,可用置换反应的原理证明氯的非金属性强于硫。反应的离子方程式为 _________________________________________。
(5)G中加入的是淀粉碘化钾溶液,发生反应的现象为_____________________________________。
(6)H为尾气处理装置,写出该装置中的离子方程式_________________________。有人认为,用NaOH溶液吸收尾气,可能会引起倒吸。下列装置中,能起到防倒吸作用的是_______(填序号字母)。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)已知咖啡酸的结构如右图所示。关于咖啡酸的描述正确的是( )
A.分子式为C9H5O4
B.1mol咖啡酸最多可与5mol氢气发生加成反应
C.与溴水既能发生取代反应,又能发生加成反应
D.能与Na2CO3溶液反应,但不能与NaHCO3溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com