
����Ŀ��(1)��ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���__________��
A��C(s)+H2O(g)=CO(g)+H2(g) ��H>0
B��2H2(g)+O2(g)=2H2O(1) ��H<0
C��NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) ��H<0
(2) ��KOH��ҺΪ�������Һ�������⣨1����ѡ��Ӧ���һ��ԭ��أ��为���ĵ缫��ӦʽΪ_______��

(3) ���ԭ���ڻ�ѧ��ҵ�����Ź㷺��Ӧ�á��ֽ�����Ƶ�ԭ���ͨ����������ͼ�е�������������aΪ���Һ��X��Y��Ϊ���Ե缫����
����aΪCuSO4��Һ������ʱ�Ļ�ѧ��Ӧ����ʽΪ___________________��
������⺬��0.04molCuSO4��0.04molNaCl�Ļ����Һ400ml������������������672 mL����״���£�ʱ����Һ��c��H+�� = _____�����������Һ������䣩��
���𰸡�B H2 - 2eһ + 2 OHһ= 2 H2O 2CuSO4+2H2O![]() 2Cu+O2+2H2SO4 0.1mol/L
2Cu+O2+2H2SO4 0.1mol/L
��������
��1������ԭ���ԭ���������Ϣ֪������Ƴ�ԭ��صķ�Ӧ�����Ƿ��ȵ�������ԭ��Ӧ��
��2����KOH��ҺΪ�������Һ������ȼ�ϵ���У������������õ��Ӻ����������ӷ�Ӧ����ˮ��
��3���ؼ�����ȷ���ԭ�����ر�����Һ�����ӵķŵ�˳����
��1������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ���ұ��������Է����е�������ԭ��Ӧ��
A.�÷�Ӧ�����ȷ�Ӧ�����Բ�����Ƴ�ԭ��أ���A����
B.�÷�Ӧ�Ƿ��ȷ�Ӧ�����Է��Ľ���������ԭ��Ӧ����������Ƴ�ԭ��أ���B��ȷ��
C.�÷�Ӧ����������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ���C����
��ѡB��
��2������Ӧ2H2(g)+O2(g)=2H2O(1) ��H<0����Ƴ�ԭ��أ��õ��Ϊȼ�ϵ�ء�����ԭ���ԭ��������������������Ӧ��������������ԭ��Ӧ��ȼ��H2�ڸ�������Ӧ����ȼ��O2���������μӷ�Ӧ�������KOH��ҺΪ�������Һ���为���缫��ӦʽΪ��H2 - 2e- + 2 OH-= 2 H2O���ʴ�Ϊ��H2 - 2e- + 2 OH-= 2 H2O��
��3���ٵ������ͭ��Һʱ����������������������������ͭ��ͬʱ��Һ���������ᣬ���Ե�ط�ӦʽΪ��2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4���ʴ�Ϊ��2CuSO4+2H2O
2Cu+O2��+2H2SO4���ʴ�Ϊ��2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4��
2Cu+O2��+2H2SO4��
����⺬��0.04mol CuSO4��0.04mol NaCl�Ļ����Һ400mL�����������������ӷŵ磬�����������������Һ�е�OH���ŵ磬�������������������ӵ����ʵ�����0.04mol��������ȫ�ŵ磬�����������0.02mol����״���µ������448mL��������ʵ��������������Ϊ672mL�������бض��������������ʵ�����0.01mol����Ӧ�й�ת�Ƶ��ӵ����ʵ�����0.08mol������������ͭ���ӷŵ磬�������Һ�е������ӷŵ硣0.04molͭ����ǡ�õõ�0.08mol���ӣ�����0.04mol����ͭ�����Ե�����Һ�е�������0.02mol�����ƺ�0.02mol���ᣬ����Һ�������ӵ�Ũ����0.04mol��0.4L��0.1mol/L���ʴ�Ϊ��0.1mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������״������(��Ҫ����![]() ������
������![]() ��CaO��
��CaO��![]() ��)���ҹ�һ����Ҫ�ij�����������Դ���Ը�����״������Ϊԭ���Ʊ����Ƚϸߵ����죬��������ͼ��ʾ������˵���������
��)���ҹ�һ����Ҫ�ij�����������Դ���Ը�����״������Ϊԭ���Ʊ����Ƚϸߵ����죬��������ͼ��ʾ������˵���������
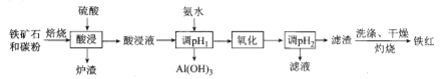
A. ������������ᡢ��ī����������ɫ��
B. ���Һ��![]() ��Һ������ɫ����
��Һ������ɫ����
C. ϴ������ʱҪ�ò��������Ͻ���
D. ����ʱѡ�õ��Լ�������![]() ��NaClO��Һ
��NaClO��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A. ��״���£�22.4L�����к��з�����ĿΪNA
B. 1mol/LNaOH��Һ�к���Na+��ĿΪNA
C. 7.8gNa2O2�к��еĹ��ۼ���ĿΪ0.1NA
D. ��0.5molN2O4�����ܱ������г�ַ�Ӧת����NO2����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ��ڹ�ҵ�����о�����Ҫ���塣
��1���ںϳɰ���ҵ��I2O5�����ڶ����ⶨCO�ĺ�������֪2I2(s)+5O2(g)=2I2O5(s) ��H=-76kJ��mol-1��2CO(g)+O2(g)=2CO2(g) ��H=-566kJ��mol-1����òⶨ��Ӧ���Ȼ�ѧ����ʽΪ____________________________________��
��2����ͬ�¶��£���װ������I2O5�����2L�����ܱ�������ͨ��4 mol CO�����CO2����������� (CO2)��ʱ��t�仯������ͼ��

��b��CO��ƽ��ת������Ϊ____________��c���ƽ�ⳣ��KΪ________________��
�����д�ʩ����߸÷�ӦCOת���ʵ���________(����ĸ)
a�������¶� b������ѹǿ c��������� d������CO2
��3������ˮ��SO2ǡ���������Σ����ʱ��Һ��_________(��������������������)����������Һ��ͨ��___________(����NH3������SO2��)��ʹ��Һ��������(��֪������NH3��H2O��Kb=1.8��10-5mol��L-1��H2SO3��Ka1=1.5��10-2mol��L-1��Ka2=6.3��10-8mol��L-1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�����½�0.2 mol/LHCl��Һ��0.2 mol/LMOH��Һ�������ϣ���û����Һ��pH��6��������Һ����ˮ�������c(H��)__________0.2 mol/LHCl��Һ����ˮ�������c(H��)��(����������������������)���û����Һ�������غ�ʽΪ ��
(2)����������0.2 mol/LMOH��Һ��0.1 mol/LHCl��Һ�������ϣ���û����Һ��pH��7����˵������ͬ������MOH�ĵ���̶�__________MCl��ˮ��̶ȡ�(����������������������)
(3)����������pH��3��HR��Һ��pH��11��NaOH��Һ�������ϣ���û����Һ��pH��7��������Һ��pH__________��(������7������7��������ȷ����)
(4)������Һ�ʼ��Ե�ԭ��(�����ӷ���ʽ��ʾ)__________________________��������Һ����Ũ���ɴ�С��˳��Ϊ ��
(5)ij�¶�ʱ�����0.01 mol/L��NaOH��ҺpHΪ11���ڴ��¶��£���pH��a��NaOH��ҺVa L��pH��b������Vb L��ϡ������û����ҺΪ���ԣ���a��12��b��2����Va ��Vb = ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫���һ��Ũ�ȵ�CuSO4��Һ��ͨ��һ��ʱ��������õ���Һ�м���0.1 mol Cu(OH)2��ǡ�ûָ������ǰ��Ũ�Ⱥ�pH��������˵����ȷ����( )
A��������������û����������
B����������ת�Ƶĵ��ӵ����ʵ���Ϊ0.4 mol
C��ԭCuSO4��Һ��Ũ��Ϊ0.1 mol��L��1
D���������������ռ������������Ϊ1.12 L(�����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ�������ʢ��1 mol PCl5�����ȵ�200��ʱ�����˷�Ӧ��PCl5(g) ![]() PCl3(g)��Cl2(g)����Ӧ�ﵽƽ��ʱPCl5�ķֽ���ΪM%������ͬһ�¶Ⱥ�ͬ�����������Ͷ�����2 mol PCl5����Ӧ�ﵽƽ��ʱPCl5�ķֽ���ΪN%��M��N�Ĺ�ϵ��(����)
PCl3(g)��Cl2(g)����Ӧ�ﵽƽ��ʱPCl5�ķֽ���ΪM%������ͬһ�¶Ⱥ�ͬ�����������Ͷ�����2 mol PCl5����Ӧ�ﵽƽ��ʱPCl5�ķֽ���ΪN%��M��N�Ĺ�ϵ��(����)
A. M>N B. M<N C. M��N D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�г���ͼ��ֱ�۵�������ѧ��Ӧ�Ľ��̻���������ͼ��������ȷ����

A. ����ͼ�ٿ��жϸÿ��淴Ӧ����ӦΪ���ȷ�Ӧ
B. ���ڱ�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g)![]() 3C(g)+D(s)��Ӱ�죬���Ҷ�Ӧ��ѹǿ��
3C(g)+D(s)��Ӱ�죬���Ҷ�Ӧ��ѹǿ��
C. ͼ�ۿɱ�ʾ������Һ��ͨ�백����������������Һ�����Եı仯
D. ����ͼ��,����ȥCuSO4�ܱ��е�Fe3+,������Һ�м�������CuO,����pH��4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д��ȷ����( �� )
A. NaHSO4��ˮ��Һ�еĵ��뷽��ʽ��NaHSO4===Na����![]()
B. H2SO3�ĵ��뷽��ʽ��H2SO3![]() 2H����
2H����![]()
C. CO![]() ��ˮ�ⷽ��ʽ��
��ˮ�ⷽ��ʽ��![]() ��H2O
��H2O![]()
![]() ��OH��
��OH��
D. CaCO3�ĵ��뷽��ʽ��CaCO3![]() Ca2����
Ca2����![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com