
【题目】在一定条件下,Na2CO3溶液存在水解平衡:CO32﹣+H2OHCO3﹣+OH﹣ . 下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.通入CO2 , 平衡朝正反应方向移动
C.升高温度, ![]() 减小
减小
D.加入NaOH固体,溶液pH减小
【答案】B
【解析】解:A、平衡常数仅与温度有关,温度不变,则稀释时平衡常数是不变的,故A错误;
B、CO2通入水中,生成H2CO3,可以与OH﹣反应,平衡正向移动,故B正确;
C、因水解是吸热的,则升温可以促进水解,平衡正向移动, ![]() 是增大的,故C错误;
是增大的,故C错误;
D、加入NaOH固体,碱性肯定增强,pH增大,故D错误;
故选:B.
【考点精析】解答此题的关键在于理解化学平衡常数的含义的相关知识,掌握指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态,以及对化学平衡移动原理以及影响因素的理解,了解影响因素:①浓度:增大反应物(或减小生成物)浓度,平衡向正反应方向移动;②压强:增大压强平衡向气体体积减小的方向移动.减小压强平衡向气体体积增大的方向移动;③温度:升高温度,平衡向吸热反应方向移动.降低温度,平衡向放热反应方向移动;④催化剂:不能影响平衡移动.


科目:高中化学 来源: 题型:
【题目】电动汽车在我国正迅猛发展,磷酸铁锂(LiFePO4)电池是电动汽车常用的一种电池,其工作原理如下图所示。中间是聚合物的隔膜把正极与负极隔开,锂离子可以通过而电子不能通过。该电池的总反应式是:LiFePO4+C6 ![]() Li1-xFePO4+LixC6 。下列说法不正确的是
Li1-xFePO4+LixC6 。下列说法不正确的是
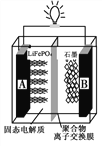
A. 放电时电子从A极通过导线流向B极
B. 充电时Li+从A极区移向B极区
C. 充电时B极电极反应式为:C6+xLi++xe-===LixC6
D. 放电时A极电极反应式为:Li1-xFePO4+xLi++ xe-=== LiFePO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类对原子结构的认识经历了一个不断深入的过程,以下科学家以及他们提出的原子结构学说(或模型)对应关系正确的是 ( )
A.道尔顿——电子轨道理论B.卢瑟福——量子力学模型
C.玻尔——行星绕太阳模型D.汤姆逊——葡萄干面包模型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ag2O2是银锌碱性电池的正极活性物质,可通过下列方法制备:在KOH加入适量AgNO3溶液,生成Ag2O沉淀,保持反应温度为80,边搅拌边将一定量K2S2O8溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品.反应方程式为
2AgNO3+4KOH+K2S2O8![]() Ag2O2↓+2KNO3+2K2SO4+2H2O
Ag2O2↓+2KNO3+2K2SO4+2H2O
回答下列问题:
(1)上述制备过程中,检验洗剂是否完全的方法是
(2)银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式: .
(3)准确称取上述制备的样品(设仅含Ag2O2和Ag2O) 2.558g,在一定的条件下完全分解为Ag 和O2,得到224.0mLO2(标准状况下).计算样品中Ag2O2的质量分数(计算结果精确到小数点后两位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的原子,其价电子排布分别为4s2、3s2 3p2 和2s2 2p4,由这三种元素组成的化合物的化学式可能是
A.XYZ2 B.X2YZ3 C.X2YZ2 D.XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 12C和14C互为同素异形体
B. 金刚石和C60互为同位素
C. CH3-CH2-CH2-CH3和![]() 互为同分异构体
互为同分异构体
D. C2H2和C6H6互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com