
【题目】铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:

完成下列填空:
(1)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式: _____Cr2O72-+Fe3O4+H+→Cr3++Fe3++H2O,_________________
(2)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:______________________
(3)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。
①回收所得的Cr(OH)3在处理之前需要先进行洗涤,洗涤沉淀的方法为____________________;
②滴定时加入的指示剂通常为________________,滴定至终点的现象是________________;
③Na2S2O3溶液的物质的量浓度为_____________________(保留四位有效数字)。
【答案】1,6,62,2,18,312CrO42-+2H+![]() Cr2O72-+H2O沿玻璃棒向漏斗中注入蒸馏水,使蒸馏水完全浸没沉淀,待蒸馏水自然流尽后,重复操作2~3次淀粉溶液溶液的颜色由蓝色变为无色,且半分钟内溶液的颜色不再改变0.2400mol·L-1
Cr2O72-+H2O沿玻璃棒向漏斗中注入蒸馏水,使蒸馏水完全浸没沉淀,待蒸馏水自然流尽后,重复操作2~3次淀粉溶液溶液的颜色由蓝色变为无色,且半分钟内溶液的颜色不再改变0.2400mol·L-1
【解析】
(1)反应中Cr2O72-→Cr3+,Cr元素由+6价降低为+3价,共降低6价,Fe3O4→Fe3+,Fe元素由平均化合价+![]() 价升高为+3价,共升高1价,化合价最小公倍数为6,Cr2O72-的系数为1,Fe3O4的系数为6,再根据原子守恒、电荷守恒配平其它物质系数,配平得反应方程式为1Cr2O72-+6Fe3O4+62H+→2Cr3++18Fe3++31H2O;
价升高为+3价,共升高1价,化合价最小公倍数为6,Cr2O72-的系数为1,Fe3O4的系数为6,再根据原子守恒、电荷守恒配平其它物质系数,配平得反应方程式为1Cr2O72-+6Fe3O4+62H+→2Cr3++18Fe3++31H2O;
(2)在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,说明黄色的CrO42-离子与离子反应产生橙色的Cr2O72-离子,该反应为可逆反应,反应式为2CrO42-+2H+![]() Cr2O72-+H2O;
Cr2O72-+H2O;
(3)①洗涤沉淀的方法为沿玻璃棒向漏斗中注入蒸馏水,使蒸馏水完全浸没沉淀,待蒸馏水自然流尽后,重复操作2~3次;②反应时碘离子被氧化为碘单质,碘遇淀粉溶液变蓝,故滴定时加入的指示剂通常为淀粉溶液,滴定至终点的现象是溶液的颜色由蓝色变为无色,且半分钟内溶液的颜色不再改变;③由测定Na2S2O3溶液的物质的量浓度的两个反应:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,可以得到关系式:Cr2O72- ~ 3I2 ~6S2O32-。0.294g K2Cr2O7 的物质的量为n(K2Cr2O7)=0.001mol ,所以n(Na2S2O3)=6 n(K2Cr2O7)=0.006mol,消耗Na2S2O3溶液25.00mL,则Na2S2O3溶液的物质的量浓度为![]() 0.2400mol·L-1。
0.2400mol·L-1。


科目:高中化学 来源: 题型:
【题目】化合物A的分子式为C9H15OCl,分子中含有一个六元环和一个甲基,环上只有一个取代基;F分子中不含甲基:A与其它物质之间的转化如下图所示:

(1)A-F的反应类型是____;G中含氧官能团的名称是____。
(2)A-C的反应方程式是________。
(3)H的结构简式是________,E的结构简式是____。
(4)有的同学认为B中可能没有氯原子,你的观点是________(填“同意”或“不同意”)你的理由_______。
(5)某烃的含氧衍生物X符合下列条件的同分异构体中,核磁共振氢谱显示为2组峰的是_____(写结构简式);只含有两个甲基的同分异构体有____种。
①相对分子质量比C少54;②氧原子数与C相同 ; ③能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
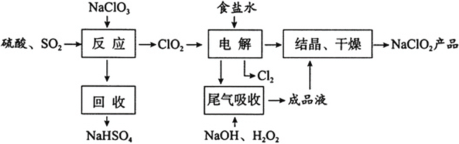
回答下列问题:
(1)NaClO2中Cl的化合价为________。
(2)写出“反应”步骤中生成ClO2的化学方程式____________________。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去杂质Ca2+和SO42-,要加入的除杂试剂顺序为_________、________。“电解”中阴极反应的主要产物是____________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为________。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到相应目的是( )
选项 | A | B | C | D |
实验 过程 |
|
|
|
|
实验 目的 | 将乙二醇(HOCH2CH2OH) 转化为乙二酸(H2C2O4) | 比较氯化铁和二氧化锰对 H2O2 分解反应的催化效果 | 证明稀硝酸与铜反应时表现出氧化性 | 用 SO2 与 Ba(NO3)2 反 应获得 BaSO3沉淀 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓H2SO4混合共热的方法制取乙酸乙酯,反应的方程式为______________________________________该反应类型______________其中浓H2SO4的作用是_________________和_________________
[装置设计]甲、乙、丙三位同学分别设计下列三套实验装置
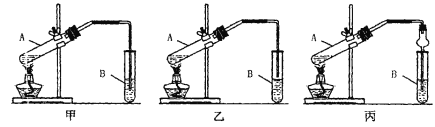
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是__________(选填“甲”或“乙”),丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是_____________
[实验步骤]①按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓H2SO4 充分摇匀,冷却后再加入2mL冰醋酸;②将试管固定在铁架台上;③在试管B中加入适量的饱和Na2CO3溶液;④用酒精灯对试管A加热;⑤当观察到试管B中有明显现象时停止实验。
[问题讨论]
(1)步骤①装好实验装置,加入样品前还应检查_________________
(2)试管B中饱和Na2CO3溶液的作用是_________________________
(3)从试管B中分离出乙酸乙酯的实验操作是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁(FeSO4·xH2O),在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x =________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”、“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

C、D中的溶液依次为BaCl2溶液、品红溶液。C、D中有气泡冒出,并可观察到的现象分别为产生白色沉淀、品红溶液褪色。写出硫酸亚铁高温分解反应的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将等物质的量的 CO 和 H2 混合气体充入恒温恒容密闭容器中进行反应:CO(g)+2H2(g)![]() CH3OH(g),下列事实能说明此反应已达到平衡状态的是
CH3OH(g),下列事实能说明此反应已达到平衡状态的是
A. 容器内气体密度保持不变B. 混合气体的平均相对分子质量不变
C. 生成 CH3OH 的速率与生成 H2 的速率相等D. CO 的体积分数保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氧化还原反应3S+6KOH=K2SO3+2K2S+3H2O中,氧化剂和还原剂的物质的量之比为( )
A.1:2B.2:1C.1:1D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构体和同系物是两个不同的概念,观察下列几种物质的化学式或结构简式,回答下列问题:
①CO(NH2)2 ②NH4CNO ③CH3CH2CH3 ④白磷(P4) ⑤ ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]() ⑨CH3CH2CH2CH3 ⑩红磷
⑨CH3CH2CH2CH3 ⑩红磷
其中,互为同素异形体的是________________;互为同分异构体的是_________________________;互为同系物的是_____________________________________;属于同种物质的是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com