
����Ŀ����ʵ�������ö������̸�Ũ���ᷴӦ�Ʊ����﴿�������������д�ʵ�飬����������ͼ��
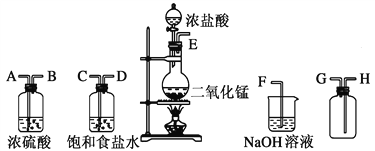
��1������������������ȷ˳��(����ӿڴ�����ĸ)____________________��
��2��װ���У�����ʳ��ˮ��������_____________________��NaOH��Һ��������____________��
��3����ѧʵ���г���ʪ��ĵ��ۣ�KI��ֽ�����Ƿ���Cl2�����������Cl2�������ɹ۲쵽________________________����Ӧ���ӷ���ʽΪ��__________________��
��4��д�����л�ѧ��Ӧ�ķ���ʽ��
�����巢��װ�ý��еķ�Ӧ��_________________��NaOH��Һ�з����ķ�Ӧ��____________
��5���������ɵ�Cl2ͨ�뵽�ֱ����и�����ɫ������ʪ����ɫ��������������ƿ�У��ῴ��ʲô���� _____________________________________��
���𰸡� E��C��D��A��B��H��G��F ��ȥ�����е��Ȼ������壬�����������ܽ�� ������������ֹ������Ⱦ ��ֽ���� 2I��+Cl2=2Cl��+I2 MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O 2NaOH+Cl2=NaCl+NaClO+H2O ʪ�����ɫ������ɫ�����������ɫ��������ɫ
MnCl2+Cl2��+2H2O 2NaOH+Cl2=NaCl+NaClO+H2O ʪ�����ɫ������ɫ�����������ɫ��������ɫ
����������1����ʵ�������ö������̸�Ũ���ᷴӦ�Ʊ����﴿������������Ҫ����װ�������������ñ���ʳ��ˮ��ȥ�Ȼ��⣬ͨ��Ũ�����ȥˮ�����������ܳ����̳��ռ����������������������Һ���ն����������װ������˳���ǣ�E��C��D��A��B��H��G��F����2������ʳ��ˮ��������ȥ�����е��Ȼ������壬�����������ܽ�ȣ�����������Һ���չ�������������ֹ��Ⱦ��������3������������������������������Ϊ���ʵ����������۱�������˿ɹ۲쵽��ֽ��������Ӧ�����ӷ���ʽΪ2I��+Cl2=2Cl��+I2����4��������װ�����Ƕ������̺�Ũ������ȷ�Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O���������ж�������������Һ���գ��������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ2NaOH+Cl2��NaCl+NaClO+H2O����5�����������û��Ư���ԣ�������ˮ��Ӧ���ɵĴ��������ǿ�����ԣ�����������ɵ�Cl2ͨ�뵽�ֱ����и�����ɫ������ʪ����ɫ��������������ƿ�У�ʵ��������ʪ�����ɫ������ɫ�����������ɫ��������ɫ��
MnCl2+Cl2��+2H2O���������ж�������������Һ���գ��������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ2NaOH+Cl2��NaCl+NaClO+H2O����5�����������û��Ư���ԣ�������ˮ��Ӧ���ɵĴ��������ǿ�����ԣ�����������ɵ�Cl2ͨ�뵽�ֱ����и�����ɫ������ʪ����ɫ��������������ƿ�У�ʵ��������ʪ�����ɫ������ɫ�����������ɫ��������ɫ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ��Ӧ���ʵ���Ҫ������(����)
A.�μӷ�Ӧ�����ʱ���������
B.����
C.�¶ȡ�ѹǿ�Լ���Ӧ��ĽӴ���
D.��Ӧ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���aLHCl��ȫ����ˮ�õ�VmL���ᣬ��Һ���ܶ�Ϊ��g��cm-3�����ʵ���������Ϊ�������ʵ����ʵ���Ũ��ΪCmolL�����������д������
A. ������CCl4��ˮ����HCl�����ܷ�����
B. ��=![]() ��100%
��100%
C. c= ![]() mol/L
mol/L
D. ������Һ���ټ���VmLˮ��������Һ����������С��0.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶Ȳ�ͬѹǿ��P1��P2���£����淴Ӧ2X��g��2Y��g��+Z��g���У�������Z�ڷ�Ӧ������е�����������ף��뷴Ӧʱ�䣨t���Ĺ�ϵ������ͼʾ����ȷ���ǣ� ��
A.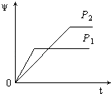
B.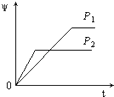
C.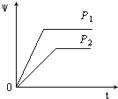
D.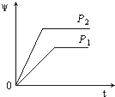
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е�һЩ���ⳣ�漰����ѧ֪ʶ��������������ȷ���� ( )
A.Ŵ���еĵ���һ������ˮ�ⷴӦ��������ɾ�
B.����������һ�����õ�ɱ������������������������ˮ
C.��������˿����Ҫ�ɷֶ�����ά��
D.����װ�β����л����ͷų��ļ�ȩ���ױ����л������Ⱦ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����500mL 2.0mol/L NaOH��Һ����0.8mol SO2��SO32- ��HSO3- �����ʵ���Ũ��֮���ǣ� ��
A. 1 : 3 B. 3��1 C. 5��4 D. 4: 5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ�У���������һ���ܹ������������
A. ��ɫ��Һ�У�Na+�� Cl-�� SO42-�� Cu2+
B. ʹ��ɫʯ����Һ������Һ�У�Na+��Ca2+��C032-��Cl
C. ��SO42-����Һ�У�K+��Ba2+��CI-��Br-
D. ������Һ�У�Na+��SO42-��Cl-��NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z����Ԫ�أ���֪����X2����Y������Y����̬�⻯����Ӿ�����ͬ�ĵ�������
��Z��Y����ɻ�����ZY3 �� ZY3��Һ�����ӳ���ɫ��
��ش�
��1��Y������������Ӧˮ����Ļ�ѧʽ�� ��
��2����ZY3��Һ�����ˮ�ɵõ����ɫҺ�壬��Ӧ�����ӷ���ʽ�� �� ��Һ����е����������������ĸ����a������ͨ����Һ��ʱ�γɹ����ġ�ͨ·��
b������缫ֱͨ�������һ������Һ����ɫ����
c�����Һ���м�����������Һ����������
d������Һ����ȡ����ɡ����պ�������������
��3��X�����ڿ�����ȼ������һ����ɫ�д̼�����ζ�����壮����֪һ�������£�ÿ1 mol�����屻O2��������98.0kJ����2 mol��������1 mol O2�ڴ������·�����Ӧ���ﵽƽ��ʱ�ų���������176.4 kJ����������ת����Ϊ ��
��ԭ��ɫ�д̼�����ζ�������뺬1.5 mol Y��һ�ֺ����ᣨ�����ij�γ�����ʵ������ȡ��������Һ��һ�������·�Ӧ��������һ��ǿ���һ�����������1.5��6.02��1023������ת��ʱ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣻���ش�����ʱ������ʹ��Ԫ�ص���ʵԪ�ط��ţ�����ʹ�����ֱ�ţ�
�� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | �� |
1 | �� | |||||||
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� |
��1���ڡ��ݡ������Ӱ뾶�ɴ�С��˳��Ϊ
��2��д���ɢ١�����Ԫ����ɣ��Ңٵ�����������ߵķ��ӵĵ���ʽ �� д���û��������ĵ��ʷ����û���Ӧ�Ļ�ѧ����ʽ ��
��3��Ԫ�آ����������ɺ�Ԫ�آݵ���������ˮ��Һ������Ӧ��д����Ӧ�����ӷ���ʽ
��4��Ԫ�آ��ж�����������м���Է���������С��Ԫ�آ��ж��ֵ��ʣ������ҵ���Է���������С����һ�������£���2L ��������1.5L ��������Ȼ�ϣ����û�����屻����NaOH ��Һ��ȫ���գ�û������������������ɵĺ������εĻ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com