
【题目】正四面体烷是一种可能存在的柏较图轻,IUPAC名称为三环[1. 1. 0. 0]丁烷。其球棍模型如图所示。下列关于该化合物的说法正确的是

A. 与环丁二烯互为同分异构体
B. 二氯代物超过两种
C. 碳碳键键角为109°28'
D. 三环[1.1. 0.0] 丁烷生成1 mol 丁烷至少需要2mol H2
【答案】A
【解析】
A.由结构可知,均含4个C、4个H;
B.4个H的位置相同;
C.4个C形成的结构与白磷结构相似;
D.三环[1.1.0.0]丁烷生成1 mol 丁烷,H原子差6mol。
A.由结构可知,正四面体烷分子式是C4H4,环丁二烯分子式也是C4H4,二者均含4个C、4个H,二者互为同分异构体,A正确;
B.正四面体烷类似一个正四面体,其四个顶点为4个C,两两以碳碳单键连接,剩余的键每个C连接一个H原子,4个H的位置相同,是一种高度对称的物质,则二氯代物只有一种,B错误;
C.4个C形成的结构与白磷结构相似,是正四面体结构,碳碳键键角为60°,C错误;
D.三环[1.1.0.0]丁烷分子式是C4H4到丁烷C4H10,1mol至少需要3mol H2,D错误;
故合理选项是A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列对文中描述内容的相关解释正确的是( )
选项 | 描述 | 解铎 |
A | 丹砂烧之成水银,积变又还成丹砂 | 两个反应互为可逆反应 |
B | 凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之 | 其中“瓦”的主要成分为硅酸盐 |
C | 硝石(KNO3)如握盐雪不冰,强烧之,紫青烟起 | 产生“紫青烟”的原因为KNO3分解 |
D | 其法用浓酒精和槽入瓶,蒸令气上,用器承滴露 | 其中涉及的操作方法为蒸发浓缩 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种形状像布袋结构的烯烃分子,其形状和结构如图所示,有关说法不正确的是( )

A. 该烯烃的分子式为C5H4
B. 该分子所有碳原子在同一平面
C. 1 mol该有机物最多可与2 mol Br2发生加成反应
D. 与其互为同分异构体且只含三键的链烃不止—种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物Z是合成某药物的中间体,其合成“片段”如下所示:

下列说法不正确的是
A. Y分子中一定有7个碳原子共平面
B. X、Y、Z分别与过量NaOH溶液反应,均生成2种产物
C. 与Z具有相同官能团的Z的同分异构体有10种
D. 有机物X能发生加成、取代、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型药物H(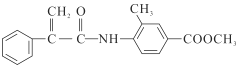 )是一种可用于治疗肿瘤的药物,其合成路线如图所示:
)是一种可用于治疗肿瘤的药物,其合成路线如图所示:

已知:
(1)E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色;
(2)RCOOH![]()
![]() ;
;
(3)![]() +R1NH2
+R1NH2![]()
![]() +HBr。(以上R,R1均为烃基)
+HBr。(以上R,R1均为烃基)
请回答下列问题:
(1)A的结构简式为___________;E的官能团的名称为___________。
(2)①的反应类型是________;④的反应条件是__________。
(3)写出C→D的化学方程式:______________________。
(4)写出F+G→H的化学方程式:_________________________________________。
(5)E有多种同分异构体,同时满足下列条件的E的同分异构体有____(考虑顺反异构)种。
i.能发生银镜反应;
ii.能发生水解反应;
iii.分子中含的环只有苯环。
(6)参照H的上述合成路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的一种重要还原剂。一般的制备方法是将AlC13溶于有机溶剂,再把所得溶液滴加到NaH粉末上,可制得铝氢化钠。实验要求和装置如下,回答下列问题:
(1)制取铝氢化钠要在非水溶液中进行,主要原因是_______(用化学方程式表示)。用下列装置制取少量铝氢化钠(含副产物处理)较为合理的是__________。

(2)对于原料A1C13的制取,某兴趣小组设计了如下装置:

①连接好装置后,应进行的第一步操作是_________;为保证产物的纯净,应待D中__________(填现象)再加热酒精灯。
②B装置中盛装饱和NaCl溶液,实验开始后B中产生的现象是_________,选择饱和NaCl溶液的理由是_____。
③C装置的作用是_________;若无C装置,试预测实验后D中生成物除A1C13外可能还含有_________。(填化学式)
④上述装置存在的明显缺陷是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,回答下列问题:
(1)该溶液中c(H+)=___________。
(2)HA的电离平衡常数K=______________;
(3)由HA电离出的c(H+)约为水电离出的c(H+)的________倍。
Ⅱ.室温下,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。
(1)如果加入蒸馏水,就加入__________mL
(2)如果加入pH = 10的NaOH溶液,应加入_________ mL
(3)如果加入0.008 mol/L HCl溶液,应加入___________ mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下,其中反应⑥发生了加聚反应。

请回答下列问题:
(1)A的结构简式为____________________,试剂a是_______________________。
(2)反应②的反应类型是___________,E中含有的官能团有___________________。
(3)反应⑥的条件是____________________________。
(4)写出E的一种具有六元环酯的同分异构体的结构简式___________________。
(5)写出由乙苯制取对溴苯乙烯(![]() )的合成路线(无机试剂任选):___________________(合成路线表示方法为:A
)的合成路线(无机试剂任选):___________________(合成路线表示方法为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。其工作流程如下:

(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。O2氧化MnO(OH)的化学方程式是_______。
(2)溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。

① 溶液a呈酸性,原因是______。
② 根据如图所示的溶解度曲线,将溶液a______(填操作),可得NH4Cl粗品。
③ 提纯NH4Cl粗品,有关性质数据如下:
化合物 | ZnCl2 | NH4Cl |
熔点 | 365℃ | 337.8℃分解 |
沸点 | 732℃ | ------------- |
根据上表,设计方案提纯NH4Cl:________。
(3)检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入_______(填试剂和现象),证明溶液中Fe3+沉淀完全。
(4)探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO2溶解的原因:________。
② 解释试剂加入顺序不同,MnO2作用不同的原因:________。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com