
【题目】雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g)![]() 2NO(g)ΔH1=a kJ·mol-1
2NO(g)ΔH1=a kJ·mol-1
②2NO(g)+O2(g)![]() 2NO2(g)ΔH2=b kJ·mol-1
2NO2(g)ΔH2=b kJ·mol-1
③CO(g)+![]() O2(g)
O2(g)![]() CO2(g)ΔH3=c kJ·mol-1
CO2(g)ΔH3=c kJ·mol-1
④2CO(g)+2NO(g)![]() N2(g)+2CO2(g)ΔH4
N2(g)+2CO2(g)ΔH4
请回答下列问题:
(1)根据反应①②③,确定反应④中ΔH4=________ kJ·mol-1。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应①的Kp=____________________________________(用表达式表示)。
(3)下列情况能说明反应②已达平衡状态的是________(填字母)。
a.单位时间内生成1 mol NO2的同时消耗了1 mol NO
b.在恒温恒容的容器中,混合气体的密度保持不变
c.在绝热恒容的容器中,反应的平衡常数不再变化
d.在恒温恒压的容器中,NO的体积分数保持不变
(4)试分析高温下不利于反应③自发进行的原因______________________________。
(5)探究反应④中NO的平衡转化率与压强、温度的关系,得到如图所示的曲线。试分析实际化工生产中不采用高压的原因______________________________。

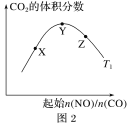
(6)探究反应④中平衡时CO2的体积分数与反应物中起始n(NO)/n(CO)的比值、温度的关系,得到如图所示的曲线。在X、Y、Z三点中,CO的转化率从大到小的顺序是____________________。
【答案】2c-a ![]() CD 因为该反应的ΔH<0,ΔS<0 常压时NO的平衡转化率已较高且高压要增加生产成本 Z>Y>X
CD 因为该反应的ΔH<0,ΔS<0 常压时NO的平衡转化率已较高且高压要增加生产成本 Z>Y>X
【解析】
(1)根据盖斯定律,反应②×2-③即得,确定反应④2CO(g)+2NO(g)![]() N2(g)+2CO2(g),据此计算焓变;
N2(g)+2CO2(g),据此计算焓变;
(2)根据反应①的方程式得出Kp=![]() ;
;
(3)化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(4)根据该反应为气体体积减小的放热反应结合△G=△H-T△S<0自发判断;
(5)根据图象分析,常压下NO的转化率已经较高,并且高压转化率增加不大,但增加成本较大,据此分析;
(6)①温度一定,随反应物NO、CO的起始物质的量比增大,X-Y反应正向进行,一氧化碳的转化率X<Y,Y-Z平衡正向进行,一氧化氮增大会提高一氧化碳的转化率,则Y<Z;
(1)根据盖斯定律,反应②×2③即得,确定反应④2CO(g)+2NO(g)N2(g)+2CO2(g)△H4=(2ca)kJ/mol;
故答案为:2ca;
(2)根据反应①的方程式得出Kp=![]() ;
;
故答案为:![]() ;
;
(3)A. 单位时间内生成1molNO2的同时消耗了lmolNO,都是正反应,故不能说明达到平衡状态,故A错误;
B.根据ρ=![]() 可知,气体总质量一定,体积一定,故密度一定,故混合气体的密度不再发生改变不能说明达到平衡状态,故B错误;
可知,气体总质量一定,体积一定,故密度一定,故混合气体的密度不再发生改变不能说明达到平衡状态,故B错误;
C. 因为平衡常数仅与温度有关,当平衡常数不再变化,即反应的温度不变,又在绝热恒容的容器中,所以反应的平衡常数不再变化能说明达到平衡状态,故C正确;
D. 在恒温恒压的容器中,NO的体积分数保持不变,则反应达平衡,能说明达到平衡状态,故D正确;
答案选CD;
(4)因为该反应为气体体积减小的放热反应,即△H<0,△S<0,所以在高温下△G=△HT△S>0非自发;
故答案为:因为该反应为气体体积减小的放热反应,即△H<0,△S<0;
(5)根据图象分析,常压下NO的转化率已经较高,并且高压转化率增加不大,但增加成本较大;
故答案为:常压下NO的转化率已经较高,并且高压要增加成本;
(6)①温度一定,随反应物NO、CO的起始物质的量比增大,XY反应正向进行,一氧化碳的转化率X<Y,YZ平衡正向进行,一氧化氮增大会提高一氧化碳的转化率,则Y<Z,X、Y、Z三点,CO的转化率的从大到小的顺序Z>Y>X;
故答案为:Z>Y>X。


科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置(如图所示),A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。按图连接装置,用酒精灯对烧瓶B加热,当观察到D中有明显现象时停止实验。试完成下列问题:
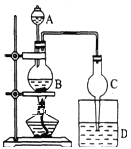
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是:___。
(2)球形干燥管除起冷凝作用外,另一重要作用是___。
(3)在该实验中,若用1mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?___,原因是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中ΔH能表示可燃物燃烧热的是 ( )
A.H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802.3kJ·mol-1
C.2H2(g)+O2(g)=2HO(g) ΔH=-571.6kJ·mol-1
D.CO(g)+![]() O2(g)=CO2(g) ΔH=-258 kJ-mol-1
O2(g)=CO2(g) ΔH=-258 kJ-mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
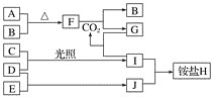
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷燃烧可以通过以下两种途径:
途径Ⅰ:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-a kJ/mol
途径Ⅱ:C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l) ΔH=-c kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-d kJ/mol (a、b、c、d 均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量 ________(填“大于 ”、“等于 ” 或“小于 ”)途径Ⅱ放出的热量。
(2)由于C3H8(g)=C3H6(g)+H2(g)的反应中,反应物具有的总能量_____(填“大于”、“等 于”或“小于 ”)生成物具有的总能量,那么在化学反应时,反应物就需要_____(填“放出 ” 或“吸收 ”)能量才能转化为生成物,因此其反应条件是____;
(3)b与a、c、d 的数学关系式是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() ,该有机物能发生( )
,该有机物能发生( )
①取代反应,②加成反应,③消去反应,④使溴水褪色,⑤使酸性KMnO4溶液褪色,⑥与AgNO3溶液生成白色沉淀,⑦聚合反应
A.以上反应均可发生B.只有⑦不能发生
C.只有⑥不能发生D.只有②不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏伽德罗定律 | |
实验方案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
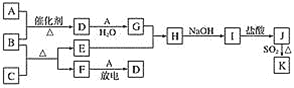
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量是化学学习的工具,请回答下列问题:
(1)标准状况下,1.7gNH3与__LH2S气体含有的氢原子数相同。
(2)VmLAl2(SO4)3溶液中含Al3+ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是___mol/L。
(3)常温常压下22.4LCO2中分子个数__64克SO2的分子个数(填“>”、“<”或“=”)。
(4)标准状况下,33.6L的NH3所含电子的物质的量约为__mol。
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为__。
(6)某盐混合溶液含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2molL-1、0.25molL-1、0.4molL-1,则c(SO42-)=___。
(7)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为___,NH3的体积分数(即NH3的体积与混合气体总体积的比值)为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com