
【题目】下列有关实验操作的叙述正确的是
A. 过滤操作中,漏斗的尖端不可接触烧杯内壁
B. 滴加试剂时,滴管的尖嘴不可接触试管内壁
C. 滴定接近终点时,滴定管的尖嘴不可接触锥形瓶内壁
D. 向容量瓶转移液体时,引流用玻璃棒不可接触容量瓶内壁
科目:高中化学 来源: 题型:
【题目】将下列物质按酸、碱、盐分类顺序排列正确的是
A. 氢氟酸、烧碱、绿矾 B. 磷酸、纯碱、芒硝
C. 石炭酸、苛性钠、醋酸钠 D. 硫酸氢钠、碱石灰、皓矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为0.1 mol·L-1的HCl溶液VmL,加水稀释到2VmL,取出10 mL,这10 mL溶液中含有c(H+)( )
A. 0.5 mol·L-1 B. 0.01 mol·L-1 C. 0.02 mol·L-1 D. 0.05 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是 ( )

A.铁是阳极,电极反应为 Fe-6e一+4H2O=FeO42-+ 8H+
B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜, 则电解结束后左侧溶液中含有FeO42-
D.电解时阳极区pH 降低、阴极区 pH升高,撤去隔膜混合后,与原溶液比较 pH升高(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)=4Na+O2↑+2H2O;后来盖· 吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:Na++e-=Na
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为2:l
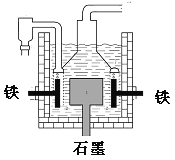
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A.石油、煤、天然气、氢气都属于化石燃料
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH<0
C.人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大
D.两个体积相同的容器中充入等量的NO2发生反应:2NO2(g)![]() N2O4(g) ΔH<0,绝热容器中气体的颜色比恒温容器中颜色深
N2O4(g) ΔH<0,绝热容器中气体的颜色比恒温容器中颜色深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
A. “可燃冰”是将水变为油的新型燃料
B. 氢气是具有热值高、无污染等优点的燃料
C. 乙醇是比汽油更环保、不可再生的燃料
D. 石油和煤是工厂经常使用的可再生的化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)当反应达到平衡时,N2和H2的浓度比是________;N2和H2的转化率比是________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量__________,密度__________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法能体现理性、低碳、环保生活理念的是( )
A. 极力反对校园垃圾,又经常使用一次性餐具
B. 夏天盖着厚被子吹空调
C. 尽量购买本地的、当季的食物,减少食物的加工过程
D. 开着大排量的家用汽车开直播声讨雾霾天气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com