
【题目】硫和锌及其化合物用途广泛。回答下列问题:
(1)基态硫原子的价电子排布图为___________。
(2)已知基态锌、铜的电离能如表所示:
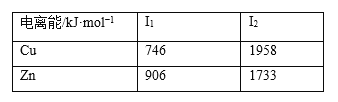
由表格数据知,I2(Cu)>I2(Zn)的原因是__________。
(3)H2O分子中的键长比H2S中的键长______(填“长”或“短”)。H2O分子的键角比H2S的键角大,其原因是_______。
(4)S8与热的浓NaOH溶液反应的产物之一为Na2S3,S32-的空间构型为_________。
(5)噻吩(![]() )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。
①噻吩分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则噻吩分子中的大π键应表示为______。
),则噻吩分子中的大π键应表示为______。
②噻吩的沸点为84 ℃,吡咯(![]() )的沸点在129~131 ℃之间,后者沸点较高,其原因是___。1 mol吡咯含____mol σ键。
)的沸点在129~131 ℃之间,后者沸点较高,其原因是___。1 mol吡咯含____mol σ键。
(6)硫化锌是一种半导体材料,其晶胞结构如图所示。
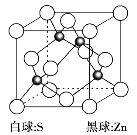
已知:硫化锌晶体密度为d g·cm3,NA代表阿伏加德罗常数的值,则Zn2和S2之间的最短核间距(x)为_________nm(用代数式表示)。
【答案】![]() Zn 失去第二个电子达到 3d10 稳定结构,而 Cu 失去第一个电子即达到稳定结构 短 氧原子半径小于硫,水分子中成键电子对之间排斥力大于 H2S V 形
Zn 失去第二个电子达到 3d10 稳定结构,而 Cu 失去第一个电子即达到稳定结构 短 氧原子半径小于硫,水分子中成键电子对之间排斥力大于 H2S V 形 ![]() 吡咯分子间存在氢键 10
吡咯分子间存在氢键 10 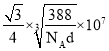
【解析】
(1)硫为16号元素,据此书写价电子排布图;
(2)Zn 为30号元素,价电子排布式为1s22s22p63s23p63d104s2, Cu为29号元素,价电子排布式为1s22s22p63s23p63d104s1,据此分析I2(Cu) >I2(Zn) 的原因;
(3)O原子半径比S原子半径小;O的电负性大于S,键合电子对偏向O,据此分析解答;
(4)根据价层电子对个数=σ键个数+孤电子对个数计算S32-的中心原子S的价层电子对数分析判断;
(5)①噻吩(![]() )分子为平面结构,环中存在两根π键,S的pz轨道中一对电子与环上的π电子共轭,形成离域大π键,据此分析解答;②吡咯环中存在N,N的电负性较S大,吡咯能形成分子间氢键;根据吡咯(
)分子为平面结构,环中存在两根π键,S的pz轨道中一对电子与环上的π电子共轭,形成离域大π键,据此分析解答;②吡咯环中存在N,N的电负性较S大,吡咯能形成分子间氢键;根据吡咯(![]() )的结构判断1 mol吡咯含有的σ键数;
)的结构判断1 mol吡咯含有的σ键数;
(6)根据均摊法计算晶胞中Zn、S原子数目,确定晶胞质量,根据晶胞的密度计算晶胞棱长,Zn2和S2之间的最短核间距(x)为体对角线长度的![]() ,据此分析计算。
,据此分析计算。
(1)硫为16号元素,最外层有6个电子,价电子排布图为![]() ,故答案为:
,故答案为:![]() ;
;
(2)Zn 为30号元素,价电子排布式为1s22s22p63s23p63d104s2,失去第二个电子达到 3d10 稳定结构,而 Cu为29号元素,价电子排布式为1s22s22p63s23p63d104s1,失去第一个电子即达到稳定结构,使得I2(Cu) >I2(Zn) ,故答案为:Zn 失去第二个电子达到 3d10 稳定结构,而 Cu 失去第一个电子即达到稳定结构;
(3)O原子半径比S原子半径小,使得H2O分子中的键长比H2S中的键长短;O的电负性大于S,键合电子对偏向O,键合电子对与键合电子对间斥力增大,键角增大,使得H2O分子中的键角∠HOH 比H2S分子中的键角∠HSH 大,故答案为:短:氧原子半径小于硫,水分子中成键电子对之间排斥力大于 H2S;
(4)单质硫与热的NaOH 浓溶液反应的产物之一为Na2S3,S32-属多硫链的一种,S32-的中心原子S的价层电子对数=2+![]() =4,采用sp3杂化,中心原子形成2个σ键、还有2个孤电子对,因此S32-的空间构型为V形,故答案为:V形;
=4,采用sp3杂化,中心原子形成2个σ键、还有2个孤电子对,因此S32-的空间构型为V形,故答案为:V形;
(5)①噻吩(![]() )分子为平面结构,环中存在两根π键,S原子价电子排布式为3s23p4,S的pz轨道中一对电子与环上的π电子共轭,形成离域大π键,形成五中心六电子的离域大π键,记为
)分子为平面结构,环中存在两根π键,S原子价电子排布式为3s23p4,S的pz轨道中一对电子与环上的π电子共轭,形成离域大π键,形成五中心六电子的离域大π键,记为![]() ,故答案为:
,故答案为:![]() ;
;
②噻吩的沸点为84℃,吡咯( ![]() )的沸点在129~131℃之间,后者沸点较高,因为吡咯环中存在N,N的电负性较S大,吡咯能形成分子间氢键使沸点升高,而噻吩分子间不能形成氢键,根据吡咯(
)的沸点在129~131℃之间,后者沸点较高,因为吡咯环中存在N,N的电负性较S大,吡咯能形成分子间氢键使沸点升高,而噻吩分子间不能形成氢键,根据吡咯(![]() )的结构可知,1 mol吡咯含有4molC-H键、1molC-C键、2molC=C键、2molC-N键、1molN-H键,共含10mol σ键,故答案为:吡咯分子间存在氢键;10;
)的结构可知,1 mol吡咯含有4molC-H键、1molC-C键、2molC=C键、2molC-N键、1molN-H键,共含10mol σ键,故答案为:吡咯分子间存在氢键;10;
(6)晶胞中Zn原子数目=4、S原子数目=8×![]() +6×
+6×![]() =4,晶胞质量=
=4,晶胞质量=![]() =
=![]() g,设晶胞棱长为 a nm,则dgcm-3×(a×10-7 cm)3=
g,设晶胞棱长为 a nm,则dgcm-3×(a×10-7 cm)3=![]() g,解得a=
g,解得a=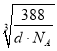 ×107 nm,Zn2和S2之间的最短核间距(x)为体对角线长度的
×107 nm,Zn2和S2之间的最短核间距(x)为体对角线长度的![]() ,因此Zn2和S2之间的最短核间距(x)为
,因此Zn2和S2之间的最短核间距(x)为![]() ×
×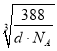 ×107 nm,故答案为:
×107 nm,故答案为:![]() ×
×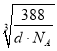 ×107 。
×107 。


科目:高中化学 来源: 题型:
【题目】碳元素形成的有机化合物在动植物体内及人类生存环境中有着相当广泛的存在,起着非常重要的作用。请结合下列有关含碳化合物的研究,完成下列填空。
(1)为了高效利用能源并且减少CO2的排放,可用下列方法把CO2转化成甲醇燃料:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=akJmol1
②2H2(g)+O2(g)=2H2O(g) △H=bkJmol1
③CH3OH(g)=CH3OH(l) △H=ckJmol1
④H2O(g)=H2O(l) △H=dkJmol1
则表示CH3OH(l)燃烧热的热化学方程式为___。
(2)用甲醇燃料电池电解处理酸性含铬废水(主要含有Cr2O72),用如图装置模拟该过程:
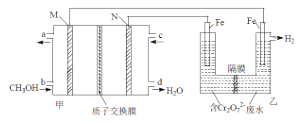
①请完成电解池中Cr2O72转化为Cr3+的离子方程式___。
②当甲池中消耗甲醇1.6g时,乙池中两电极的质量差为___g。
(3)葡萄糖和果糖为同分异构体,在一定条件下,C6H12O6(葡萄糖)![]() C6H12O6(果糖) △H﹤0。该反应的速率方程式可表示为v(正)=k(正)c(葡)、v(逆)=k(逆)c(果),k(正)和k(逆)在一定温度下为常数,分别称作正、逆反应速率常数。T1温度下,k(正)=0.06s1,k(逆)=0.002s1。
C6H12O6(果糖) △H﹤0。该反应的速率方程式可表示为v(正)=k(正)c(葡)、v(逆)=k(逆)c(果),k(正)和k(逆)在一定温度下为常数,分别称作正、逆反应速率常数。T1温度下,k(正)=0.06s1,k(逆)=0.002s1。
①T1温度下,该反应的平衡常数K1=___。
②该反应的活化能Ea(正)___Ea(逆)(填“大于”、“小于”或“等于”)。
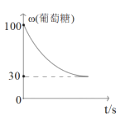
③该T2温度下,从开始反应到平衡的过程中,葡糖糖的质量分数变化如图所示。可以确定温度T2___T1(填“大于”、“小于”或“等于”)。
(4)H2A为二元弱酸。室温下配制一系列c(H2A)+c(HA)+c(A2)=0.100molL1的H2A与NaOH的混合溶液。测得H2A、HA、A2的物质的量分数c(x)%(c(x)%=![]() ×100%)随pH变化如图所示。
×100%)随pH变化如图所示。
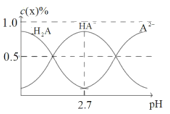
①当c(Na+)=0.100molL1时,溶液中离子浓度的大小顺序为___。
②室温下,若将0.100molL1的H2A与amolL1的NaOH溶液等体积混合,使溶液的pH=7。则H2A的Ka2=___molL1(用a表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PHB树脂可用于制作外科手术缝合线,有机物K是一种抗惊厥药物,它们的合成路线如图:
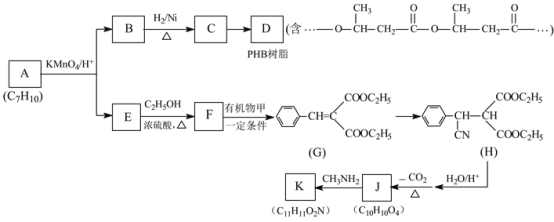
已知:
①RCN![]() RCOOH
RCOOH
②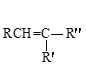
![]() RCOOH+
RCOOH+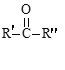
③RCHO+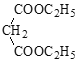
![]()
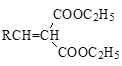 + H2O
+ H2O
R、R′、R″代表烃基
(1)有机物甲的结构简式为____________。
(2)写出一定条件下C→D的化学方程式:____________。
(3)写出E→F的化学方程式:__________________。
(4)A的结构简式为______________。
(5)已知1 mol J最多与2 mol NaHCO3反应;K分子结构中含有一个五元环与一个六元环。写出一定条件下J→K的化学方程式:____________。
(6)S是A的一种同分异构体,分子中没有环状结构,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为___________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
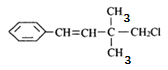
A.该有机物有三种官能团
B.1mol该有机物能与H2发生反应,消耗H2物质的量为4mol
C.一定条件下,能发生加聚反应
D.该有机物苯环上的一个H被取代,有3种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:溴苯的熔点为30.8℃,沸点156℃。实验室用苯和液溴制取溴苯的装置如图:
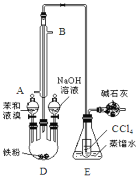
(1)冷凝管的作用___。
(2)E中小试管内CCl4作用___。
(3)用实验证明制取溴苯的反应是取代反应还需添加的试剂是___。
(4)写出图中装有碱石灰的仪器的名称___。
(5)苯与溴还可能发生副反应生成对二溴苯(沸点220℃)和邻二溴苯(沸点224℃),在实验得到的溴苯中还含有二溴苯,可通过___(填分离方法)提纯得到溴苯,写出生成对二溴苯的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
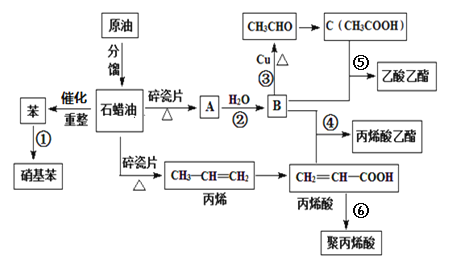
(1)丙烯酸中含氧官能团的名称为___。
(2)写出下列反应的反应类型⑤___;⑥___。
(3)下列说法正确的是(__________)
A.硝基苯中混有浓HNO3和H2SO4,将其倒入到NaOH溶液中,静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.聚丙烯酸能够使酸性高锰酸钾溶液褪色
D.有机物C与丙烯酸属于同系物
(4)写出下列反应方程式:
③B→CH3CHO___。
④丙烯酸+B→丙烯酸乙酯___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四甲基氢氧化铵[(CH3)4NOH]是一元强碱。常温下,向20mL、浓度均为0.1mol·L-1的四甲基氢氧化铵溶液、氨水中分别滴加0.1mol·L-1盐酸,溶液导电性如图所示(已知:溶液导电性与离子浓度相关)。下列说法正确的是
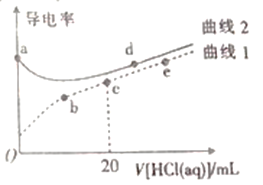
A. 在a、b、c、d、e中,水电离程度最大的点是d
B. c点溶液中:c(H+)=c(OH-)+c(NH3·H2O)
C. 曲线I中c与e之间某点溶液呈中性
D. a点溶液pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是:
A. 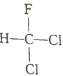 和
和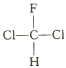 互为同分异构体
互为同分异构体
B. 15g甲基(﹣CH3)含有的电子数是9NA
C. 7.8g苯中含有的碳碳双键数为0.3NA
D. 标准状况下,2.24 L CCl4中的原子总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com