
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
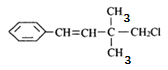
A.该有机物有三种官能团
B.1mol该有机物能与H2发生反应,消耗H2物质的量为4mol
C.一定条件下,能发生加聚反应
D.该有机物苯环上的一个H被取代,有3种同分异构体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】写出下列有机物的系统命名或结构简式:
(1) ![]() _________________
_________________
(2)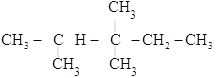 ________________
________________
(3)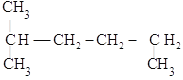 __________
__________
(4)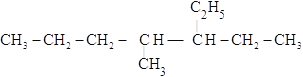 ______________
______________
(5)2,2-二甲基-3-乙基己烷____________________
(6)1,1,2,2-四氯丙烷____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是
A. CS2为V形的极性分子
B. ClO3—的空间构型为平面三角形
C. SF6中有6对相同的成键电子对
D. SiF4和SO32—的中心原子均为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在___对自旋相反的电子,基态氮原子的价层电子排布图为____。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为__其中氧原子的杂化方式为_______。
(3)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(![]() )中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A. 电解质溶液中混入水,对电池反应无影响
B. 金属锂作电池的正极,石墨作电池的负极
C. 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D. 电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___。
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
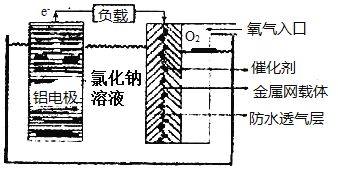
该电池的正极反应方程式为___,当铝电极质量减少9克,则另一极通入的氧气的体积在标准状况下为___。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为___。
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为___,相同压强下,AsH3的沸点___NH3(填“大于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和锌及其化合物用途广泛。回答下列问题:
(1)基态硫原子的价电子排布图为___________。
(2)已知基态锌、铜的电离能如表所示:
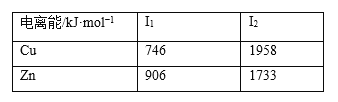
由表格数据知,I2(Cu)>I2(Zn)的原因是__________。
(3)H2O分子中的键长比H2S中的键长______(填“长”或“短”)。H2O分子的键角比H2S的键角大,其原因是_______。
(4)S8与热的浓NaOH溶液反应的产物之一为Na2S3,S32-的空间构型为_________。
(5)噻吩(![]() )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。
①噻吩分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则噻吩分子中的大π键应表示为______。
),则噻吩分子中的大π键应表示为______。
②噻吩的沸点为84 ℃,吡咯(![]() )的沸点在129~131 ℃之间,后者沸点较高,其原因是___。1 mol吡咯含____mol σ键。
)的沸点在129~131 ℃之间,后者沸点较高,其原因是___。1 mol吡咯含____mol σ键。
(6)硫化锌是一种半导体材料,其晶胞结构如图所示。
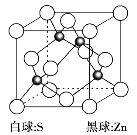
已知:硫化锌晶体密度为d g·cm3,NA代表阿伏加德罗常数的值,则Zn2和S2之间的最短核间距(x)为_________nm(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代在冶炼金属方面成就显著,请回答:
(1)商代司母戊鼎属于_____(选填“青铜”、“铁合金”或“铝合金”)制品。
(2)下图为铜及其化合物之间的转化关系(反应条件略去):
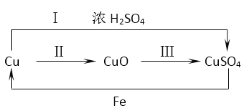
①上述转化常伴随颜色的变化,紫红色的铜与氧气反应生成______色的氧化铜;
②“曾青得铁则化为铜”体现了我国古代湿法炼铜的原理,其中的反应有:Fe + CuSO4 = FeSO4 + Cu,由此可知铁比铜的金属活动性________(选填写“强”或“弱”);
③为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是_______;
④由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径________(选填“甲”或“乙”),理由是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙胺是一种一元碱,碱性比一水合氨稍强,在水中电离方程式为![]() 。
。![]() 时,在
时,在![]() 乙胺溶液中滴加
乙胺溶液中滴加![]() 盐酸
盐酸![]() ,混合溶液的
,混合溶液的![]() 与
与 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )
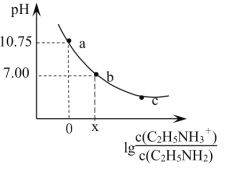
A.在![]() 时加水稀释混合溶液,b点向c点移动
时加水稀释混合溶液,b点向c点移动
B.b点对应溶液中离子浓度关系:![]()
C.在a点时,![]()
D.![]() 时乙胺的电离常数
时乙胺的电离常数![]() 的数量级为
的数量级为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com