
【题目】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___。
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
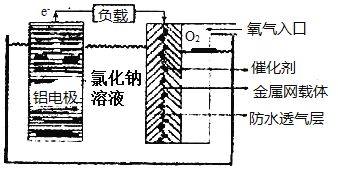
该电池的正极反应方程式为___,当铝电极质量减少9克,则另一极通入的氧气的体积在标准状况下为___。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为___。
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为___,相同压强下,AsH3的沸点___NH3(填“大于”或“小于”)。
【答案】4Al+3O2=2Al2O3,表面能形成致密的氧化膜,能保护内层金属不被氧化 O2+4e-+2H2O=4OH- 5.6L AlCl3+3NaN3![]() 3NaCl+4N2↑+AlN
3NaCl+4N2↑+AlN ![]() 小于
小于
【解析】
(1) 铝属于活泼金属却能在空气中稳定存在,是因为铝在空气中能与氧气发生反应4Al+3O2=2Al2O3,生成的氧化铝是致密的氧化膜,能够有效的阻止内部的铝继续被氧化,故答案为:4Al+3O2=2Al2O3,表面能形成致密的氧化膜,能保护内层金属不被氧化;
(2)铝—空气电池,氯化钠溶液为中性电解质溶液,铝作负极发生反应:![]() ,空气中的氧气在正极发生反应:O2+4e-+2H2O=4OH-,当铝电极质量减少9克时,由电极反应可知铝失电子物质的量为
,空气中的氧气在正极发生反应:O2+4e-+2H2O=4OH-,当铝电极质量减少9克时,由电极反应可知铝失电子物质的量为![]() ,根据电子得失守恒可得消耗氧气物质的量为
,根据电子得失守恒可得消耗氧气物质的量为![]() ,标准状况下氧气的体积为
,标准状况下氧气的体积为![]() ,故答案为:O2+4e-+2H2O=4OH-;5.6L;
,故答案为:O2+4e-+2H2O=4OH-;5.6L;
(3) AlCl3与NaN3在高温下反应得氮化铝(AlN)和N2,根据原子守恒还有氯化钠生成,反应方程式为AlCl3+3NaN3![]() 3NaCl+4N2↑+AlN,故答案为:AlCl3+3NaN3
3NaCl+4N2↑+AlN,故答案为:AlCl3+3NaN3![]() 3NaCl+4N2↑+AlN;
3NaCl+4N2↑+AlN;
(4) AsH3分子的电子式为![]() ,相同压强下,NH3分子间存在氢键,氢键作用大于分子间作用力,导致NH3沸点大于AsH3的沸点,
,相同压强下,NH3分子间存在氢键,氢键作用大于分子间作用力,导致NH3沸点大于AsH3的沸点,
故答案为:![]() ;小于;
;小于;


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确且与对应操作和目的相符的是
选项 | 目的 | 操作 | 离子方程式 |
A | 比较Fe2+和Br还原性强弱 | 向FeBr2溶液中加入少量氯水 | 2Br+Cl2=Br2+2Cl |
B | 比较C、Si非金属性强弱 | 向硅酸钠溶液中通入少量二氧化碳 | SiO32-+CO2+H2O=H2SiO3↓+ CO32- |
C | 除去CO2中的SO2 | 将气体通入盛有饱和碳酸氢钠溶液的洗气瓶 | CO32-+SO2=SO32-+CO2 |
D | 实验室制取氯气 | 向MnO2固体中加入浓盐酸并加热 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
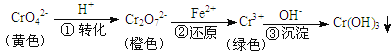
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)![]() Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
下列有关说法不正确的是
A.步骤①中当v正(CrO42—)=2v逆(Cr2O72—)时,说明反应:2CrO42—+2H+![]() Cr2O72—+H2O达到平衡状态
Cr2O72—+H2O达到平衡状态
B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原1 mol Cr2O72—离子,需要12 mol (NH4)2Fe(SO4)2
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+)≤10-5mol/L时,可视作该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂钒氧化物电池的能量密度远远超过其他材料电池,其成本低,便于大量推广,且对环境无污染。已知电池的总反应为V2O5+xLi![]() LixV2O5,下列说法正确的是
LixV2O5,下列说法正确的是
A. 电池在放电时,Li+向电源负极移动
B. 充电时阳极的反应为LixV2O5-xe-===V2O5+xLi+
C. 放电时负极失重7.0 g,则转移2 mol电子
D. 该电池以Li、V2O5为电极,酸性溶液作介质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
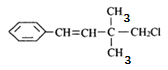
A.该有机物有三种官能团
B.1mol该有机物能与H2发生反应,消耗H2物质的量为4mol
C.一定条件下,能发生加聚反应
D.该有机物苯环上的一个H被取代,有3种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_____;Ti原子核外共有________种运动状态不同的电子。
(2)BH3分子与NH3分子的空间结构分别为_________;BH3与NH3反应生成的BH3·NH3分子中含有的化学键类型有_______,在BH3·NH3中B原子的杂化方式为________。
(3)N和P同主族。科学家目前合成了N4分子,该分子中N—N—N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途___________。(写出一种即可)
(4)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是____。
(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图所示。化合物乙的沸点明显高于化合物甲,主要原因是______。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为________。
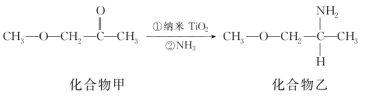
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
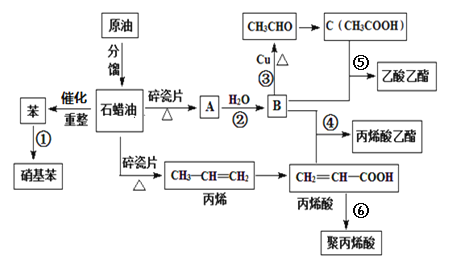
(1)丙烯酸中含氧官能团的名称为___。
(2)写出下列反应的反应类型⑤___;⑥___。
(3)下列说法正确的是(__________)
A.硝基苯中混有浓HNO3和H2SO4,将其倒入到NaOH溶液中,静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.聚丙烯酸能够使酸性高锰酸钾溶液褪色
D.有机物C与丙烯酸属于同系物
(4)写出下列反应方程式:
③B→CH3CHO___。
④丙烯酸+B→丙烯酸乙酯___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 常温常压下,4.6 g NO2气体约含有1.806×1023个原子
B. 标准状况下,80 g SO3所占的体积约为22.4 L
C. 标准状况下,22.4 L CCl4中含有的CCl4分子数为NA
D. 标准状况下,22.4 L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种常用的抗组胺药物,一种合成路线如下:

已知:①C为最简单的芳香烃,且A、C互为同系物。
②2ROH+NH3![]() HNR2+2H2O(R代表烃基)。
HNR2+2H2O(R代表烃基)。
请回答下列问题:
(1)A的化学名称是___,H中的官能团名称是_______。
(2)由E生成F的反应类型是______,G的结构简式为______。
(3)A→B的化学方程式为_____。
(4)L是F的同分异构体,含有联苯(![]() )结构,遇FeCl3溶液显紫色,则L有___种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为_____。
)结构,遇FeCl3溶液显紫色,则L有___种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为_____。
(5)写出用氯乙烷和2-氯-1-丙醇为原料制备化合物![]() 的合成路线(其他无机试剂任选)。____
的合成路线(其他无机试剂任选)。____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com