
【题目】生产生活中的化学电源、金属冶炼、环境污染等都与氧化还原反应息息相关,研究氧化还原反应,对人类进步和社会发展都具有极其重要的意义。
(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑
①通过观察以上两个反应,对其中Fe2+的认识是 __________________。
②I2和Fe2+一样也能与H2O2发生上述类似反应,类比上述反应,在下面空格上填入合适的化学方程式:H2O2+I2= 2HIO;___________。总的化学方程式为_____________________________。
(2)2017年4月1日,中共中央、国务院印发通知,决定设立河北雄安新区。据报道周边污水渗坑给雄安新区的水环境带来隐患,目前采用多种方法对污水进行处理,改善水资源状况。
①碱性环境下,Cl2可将水中残存的CN-转化为两种无毒的气体,则该反应生成两种无毒气体的物质的量之比为_________________。
②酸性环境下,向含重铬酸根(Cr2O72-)的废水中加入FeSO4溶液,然后调节溶液pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应对应的离子方程式________________________________。
【答案】 其为过氧化氢分解的催化剂 2HIO+H2O2=I2+2H2O+O2↑ 2H2O2![]() 2H2O+O2↑ 2:1或1:2 Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
2H2O+O2↑ 2:1或1:2 Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
【解析】(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑,①通过观察以上两个反应,将两方程式相加,得2H2O2=2H2O+O2↑,对其中Fe2+的认识是反应的催化剂;②用总反应2H2O2=2H2O+O2↑减去H2O2+I2= 2HIO得2HIO+H2O2=I2+2H2O+O2↑ ;总的化学方程式为2H2O2![]() 2H2O+O2↑ ;(2)2CN-+8OH-+5Cl2=2CO2+N2+10Cl-+4H2O,生成两种无毒气体CO2和N2的物质的量之比为2:1;在酸性环境下,酸性环境下能够氧化二价铁离子生成三价铁离子,本身被还原为三价铬离子,反应的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
2H2O+O2↑ ;(2)2CN-+8OH-+5Cl2=2CO2+N2+10Cl-+4H2O,生成两种无毒气体CO2和N2的物质的量之比为2:1;在酸性环境下,酸性环境下能够氧化二价铁离子生成三价铁离子,本身被还原为三价铬离子,反应的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】若将15P原子的电子排布式写成1s22s22p63s23px23py1,它违背了
A.能量最低原则B.泡利不相容原理
C.洪特规则D.能量守恒原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
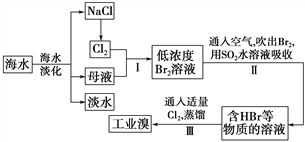
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
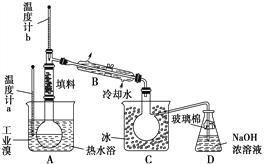
请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的N2、H2气体充入某密闭容器中,在一定条件下发生反应并达到平衡:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是( )
2NH3(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是( )
选项 | 改变条件 | 新平衡与原平衡比较 |
A | 增大压强 | N2的浓度一定变小 |
B | 升高温度 | N2的转化率变小 |
C | 充入一定量H2 | H2的转化率不变,N2的转化率变大 |
D | 使用适当催化剂 | NH3的体积分数增大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去乙酸乙酯中残留的乙酸,有效的处理方法是
A. 蒸馏 B. 用过量饱和碳酸钠溶液洗涤后分液
C. 水洗后分液 D. 用过量的氢氧化钠溶液洗涤后分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列物理量不再发生变化时:
①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量
(1)能说明2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡状态的是____________。
2SO3(g)达到平衡状态的是____________。
(2)能说明I2(g)+H2(g) ![]() 2HI(g)达到平衡状态的是_______________。
2HI(g)达到平衡状态的是_______________。
(3)能说明2NO2(g) ![]() N2O4(g)达到平衡状态的是______________________。
N2O4(g)达到平衡状态的是______________________。
(4)能说明C(s)+CO2(g) ![]() 2CO(g)达到平衡状态的是_________________。
2CO(g)达到平衡状态的是_________________。
(5)能说明NH2COONH4(s) ![]() 2NH3(g)+CO2(g)达到平衡状态的是__________。
2NH3(g)+CO2(g)达到平衡状态的是__________。
(6)能说明5CO(g)+I2O5(s) ![]() 5CO2(g)+I2(s)达到平衡状态的是________。
5CO2(g)+I2(s)达到平衡状态的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖是一种单糖的主要原因是( )
A. 糖类中含碳原子数量最少 B. 糖类中结构最简单
C. 分子中只有一个醛基 D. 不能再水解成更简单的糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com