
抗击“非典”期间,过氧乙酸是广为使用的消毒剂,它可由H2O2和、冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0涉及下列反应:
① MnO4-
+
MnO4-
+ H2O2
+
H2O2
+ H+
═
H+
═ Mn2+ +
Mn2+ + O2
+
O2
+  H2O
H2O
② H2O2 + 2I- + 2 H+ ═ I2 + 2 H2O
③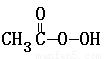 + 2I-
+ 2 H+ ═ CH3COOH + I2
+ 2 H2O
+ 2I-
+ 2 H+ ═ CH3COOH + I2
+ 2 H2O
④I2 + 2S2O32- ═ S4O62- + 2 I-
请回答下列问题:
(1)配平反应①的离子方程式:
 MnO4-
+
MnO4-
+ H2O2
+
H2O2
+ H+
═
H+
═  Mn2++
Mn2++
 O2 +
O2 +  H2O
H2O
(2)用Na2S2O3标准溶液滴定I2是(反应④)选用的指示剂是 。
(3)取b0mL待测液,用硫酸使溶液酸化,再用浓度为a1mol·L-1的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
另取b0mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(适应②和③)。再用浓度为a2mol·L-1的Na2S2O3标准溶液滴定生成的I2,,耗用Na2S2O3的体积为b2mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、 b1 、b2 、b0的代数表示)
c0 = .
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有
准确称量,是否影响测定结果 (填是或否)。
(1) 2 5 6 2 5 8 (3分) (2) 淀粉溶液 (2分)
(3) 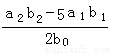 (3分) (4)否
(2分)
(3分) (4)否
(2分)
【解析】(1)反应中Mn的化合价从+7价降低到+2价,得到2个电子。双氧水中氧元素的化合价从-1价升高到0价,失去1个电子,所以根据电子得失守恒可知,氧化剂和还原剂的物质的量之比是2︰5,则方程式中系数分别是2 5 6 2 5 8。
(2)由于碘单质能和淀粉发生显色反应,所以指示剂是淀粉。
(3)根据反应①可知溶液中含有双氧水是0.0025a1b1mol,则根据反应②可知双氧水氧化生成的碘单质是0.0025a1b1mol。根据反应④可知生成的碘单质根据是0.0005a2b2mol,所以由过氧乙酸生成的碘单质是0.0005a2b2mol-0.0025a1b1mol,因此根据反应③可知过氧乙酸的物质的量是0.0005a2b2mol-0.0025a1b1mol,所以其浓度是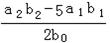
(4)根据(3)可知,反应是过量的碘化钾不参与反应,所以不影响结果。


科目:高中化学 来源: 题型:


| a2b2-5a1b1 |
| 2b0 |
| a2b2-5a1b1 |
| 2b0 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:043
抗击:“非典”期间,过氧乙酸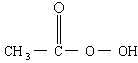 是广为使用的消毒剂.它可由
是广为使用的消毒剂.它可由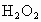 和冰醋酸反应制取,所以在过氧乙酸中常含有残留的
和冰醋酸反应制取,所以在过氧乙酸中常含有残留的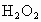 .测定产品中过氧乙酸浓度
.测定产品中过氧乙酸浓度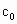 .涉及下列反应:
.涉及下列反应:
①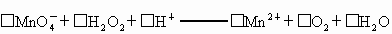
②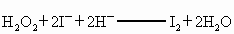
③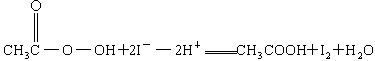
④
请回答以下问题:
(1)配平反应①的离子方程式(配乎化学计量数填入以下方框内):

(2)用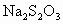 标准溶液滴定
标准溶液滴定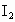 时(反应④)选用的指示剂是__________.
时(反应④)选用的指示剂是__________.
(3)取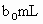 待测液,用硫酸使溶液酸化,再用浓度为
待测液,用硫酸使溶液酸化,再用浓度为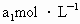 标准溶液滴定其中的
标准溶液滴定其中的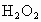 ,耗用的
,耗用的 体积为
体积为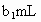 (反应①,滴定过程中
(反应①,滴定过程中 不与过氧乙酸反应).
不与过氧乙酸反应).
另取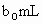 待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的
待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的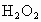 都能跟KI反应生成
都能跟KI反应生成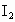 (反应②和③).再用浓度为
(反应②和③).再用浓度为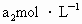 的
的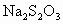 标准溶液滴定生成的
标准溶液滴定生成的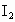 ,耗用
,耗用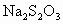 溶液体积为
溶液体积为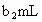 .
.
请根据上述实验数据计算过氧乙酸的浓度(用含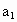 、
、 、
、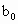 、
、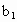 、
、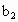 的代数式表示).
的代数式表示).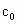 =__________.
=__________.
(4)为计算待测液中过氧乙酸的浓度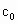 ,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).
,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).
查看答案和解析>>
科目:高中化学 来源: 题型:
①_____![]() +_____H2O2+______H+——_____Mn2++______O2+______H2O
+_____H2O2+______H+——_____Mn2++______O2+______H2O
②H2O2+2I-+2H+====I2+2H2O
③CH3COOOH+2I-+2H+====CH3COOH+I2+H2O
④I2+2![]() ====S4O62-+2I-
====S4O62-+2I-
请回答以下问题:
(1)配平反应①的离子方程式(配平化学计量数依次填在下面所给直线上):
![]() +_____H2O2+_____H+——______Mn2++_____O2+_____H2O
+_____H2O2+_____H+——______Mn2++_____O2+_____H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是________。
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol·L-1的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中,KMnO4不与过氧乙酸反应)。
另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(反应②和③)。再用浓度为a2 mol·L-1的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度。
c0=________(用含a1、a2、b0、b1、b2的代数式表示)。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果______(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源:2013届安徽省太湖二中高三上学期期末前月考化学试卷(带解析) 题型:填空题
抗击“非典”期间,过氧乙酸( )是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
① □MnO4+□H2O2+□H+ ═□Mn2++□O2十□H2O
② H2O2+2 +2H+ ═ I2+2H2O
+2H+ ═ I2+2H2O
④ I2+2S2O32-═S4O62-+2I-
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填人以下方框内):
□MnO-4+□H2O2+□H+ ═ □Mn2++□O2十□H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是_____________________。
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol· 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KmnO4不与过氧乙酸反应)。另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol·
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KmnO4不与过氧乙酸反应)。另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol· 的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。
c0= ________________________。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 _______________(填是或否)
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省高三下学期第一次模拟考试化学试卷 题型:填空题
(8分)抗击“非典”期间,过氧乙酸( 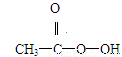 )是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
① □MnO4-+□H2O2+□H+ = □Mn2++□O2十□H2O
②
H2O2+2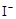 +2H+ = I2+2H2O
+2H+ = I2+2H2O
③
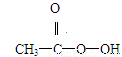 +2
+2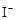 +2H+ = CH3COOH+I2+H2O
+2H+ = CH3COOH+I2+H2O
④ I2+2S2O32- = 2I-+S4O62-
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填人以下方框内):
MnO4-+ H2O2+ H+ === Mn2++ O2十 H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是________________________
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol·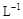 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2
mol·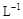 的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。
c0= ___________ 。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 _______________(填是或否)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com