
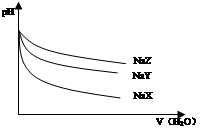
| A.在上述三种盐原溶液中,水的电离度大小是NaX>NaY>NaZ |
| B.在等物质的量浓度的NaX、NaY、NaZ混合液中,离子浓度的大小关系是c(Z-)>c(Y-)>c(X-) |
| C.在上述NaX和NaY的混合液中存在c(HX)/c(X-)=c(HY)/c(Y-) |
| D.在0.2mol·L-1 NaX溶液中加入等体积0.1mol·L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
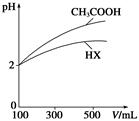
| A.多元弱酸的酸性主要由第一步电离决定,亚硫酸的酸性弱于碳酸 |
| B.多元弱酸的酸性主要由第二步电离决定,碳酸的酸性弱于亚硫酸 |
| C.多元弱酸的酸性主要由第一步电离决定,亚硫酸的酸性强于碳酸 |
| D.多元弱酸的酸性主要由第二步电离决定,碳酸的酸性强于亚硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HBr、HCl、BaSO4 |
| B.NH4Cl、CH3COOH、Na2S |
| C.NaOH、Ca(OH)2、NH3·H2O |
| D.HClO、NaF、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AlCl3溶液中再溶入AlCl3 |
| B.CH3COONa溶液加热 |
| C.氨水中加入少量NH4Cl固体 |
| D.醋酸溶液加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合前:pH(CH3COOH)+pH(NaOH)=14 |
| B.混合后:c(Na+)=c(CH3COO-)+c(OH-) |
| C.混合前:c(CH3COOH)>c(NaOH) |
| D.混合后:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
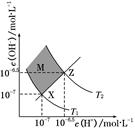
| A.两条曲线间任意点均有c(H+)×c(OH-)=KW |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
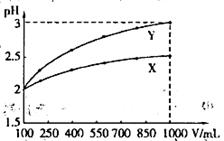
A.X为弱酸,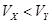 | B.Y为强酸,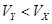 |
C.X为强酸,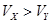 | D.Y为弱酸,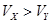 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com