
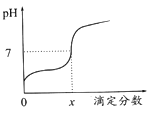
【题目】常温下,用0.1mol/L的NaOH溶液滴定相同浓度的一元弱酸HA20mL,滴定过程中溶液的pH随滴定分数(滴定分数= ![]() ) 的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
) 的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
A. HA溶液加水稀释后,溶液中c(HA)/c(A-)的值减少
B. 当滴定分数为1时,溶液中水的电离程度最大
C. 当滴定分数大于1时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)> c(H+)
D. 当滴定分数为x时,HA的电离常数为KHA=(10-7x)/(1-x)
科目:高中化学 来源: 题型:
【题目】某主族元素R的最高正化合价与最低负化合价的代数和为4,下列有关叙述正确的是
A.R一定是第4周期元素
B.R的气态氢化物化学式为H2R
C.R的气态氢化物比同周期其他元素的气态氢化物稳定
D.R的气态氢化物的水溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素最外层电子数与原子序数的关系图. 
请回答下列问题:
(1)画出Z的原子结构示意图 .
(2)原子半径:YZ(填“>”、“<”).
(3)Y的最高价氧化物的水化物与氢氧化钠溶液反应的化学方程式为 .
(4)X的最高价氧化物的水化物的化学式为 .
(5)画出W的氢化物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空.
(1)乙烯的产量常作为的标志,写出乙烯的一种用途 .
(2)写出高分子 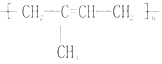 的名称 , 其单体的结构简式 .
的名称 , 其单体的结构简式 .
(3)壬烷有多种同分异构体,其中一种同分异构体不能由烯烃加成得到,写出这种同分异构体结构简式 .
(4)有机物C8H8的一种同分异构体1H﹣﹣NMR谱中只有一个信号,且能使溴水褪色,写出其结构简式 .
(5)有机物C7H15Br的一种同分异构体与氢氧化钠的乙醇溶液共热可得到三种烯烃,写出这种同分异构体的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)═3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.vA=0.5molL﹣1s﹣1
B.vB=0.3 molL﹣1s﹣1
C.vC=0.8 molL﹣1s﹣1
D.vD=1.0 molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置中,观察到电流计指针偏转,M棒变粗,N棒变细,并测得电解质溶液的质量减小,由此判断下表中所列M、N、P物质,其中可以成立的是( )

M | N | P | |
A | Zn | Cu | 稀硫酸溶液 |
B | Cu | Fe | 稀盐酸 |
C | Ag | Zn | 硝酸银溶液 |
D | Zn | Fe | 硫酸亚铁溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( ) 
A.由MgCl2制取Mg是放热过程
B.热稳定性:MgI2>MgBr2>MgCl2>MgF2
C.常温下氧化性:F2<Cl2<Br2<I2
D.由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(g),△H=﹣117kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2﹣二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验中可以用图9所示装置制备1,2﹣二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水).请填写下列空白:
(1)烧瓶a要求温度迅速升高到170℃发生反应,写出该反应的化学方程式;该反应类型为 .
(2)写出制备1,2﹣二溴乙烷的化学方程式 .
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象 .
(4)容器c中NaOH溶液的作用是;e装置内NaOH溶液的作用是 .
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因(至少2点) . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com