
| A、5条 | B、6条 | C、7条 | D、8条 |


科目:高中化学 来源: 题型:
| A、“另一种反应物”一定具有还原性 |
| B、CuH既可做氧化剂也可做还原剂 |
| C、CuH+Cl2═CuCl+HCl(燃烧) |
| D、CuH+HCl═CuCl+H2↑(常温) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下可以用H2除去乙烷中混有的乙烯 |
| B、苯和四氯化碳都能萃取溴水中的溴 |
| C、乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法分离 |
| D、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答下列问题:
某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
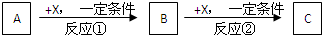
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质硫在空气中燃烧可生成SO2 |
| B、SO2能使品红溶液褪色是因为它具漂白性,加热可恢复原本红色 |
| C、SO2和Cl2都具有漂白作用,所以将两种气体等物质的量同时作用于潮湿有色物,可增强漂白作用 |
| D、SO2能使加酚酞的NaOH溶液褪色是因为它能与NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B、向AgCl悬浊液中滴入KI溶液有AgI沉淀生成,说明AgCl的溶解度小于AgI的溶解度 |
| C、0.2 mol/L HCl溶液与等体积0.05 mol/L Ba(OH)2 溶液混合后,溶液的pH=1 |
| D、0.2 mol/L的NaHCO3溶液中c(H-)+c(Na+)=c(CO32-)+c(OH-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
| A、离子晶体中阳离子的半径越大,越易分解 |
| B、离子晶体中阳离子的半径越小,越易分解 |
| C、离子晶体中阳离子的半径越大,结合碳酸根中的氧离子越容易 |
| D、离子晶体中阳离子的半径越小,结合碳酸根中的氧离子越容易 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com