
【题目】下列图示与对应的叙述相符的是( )
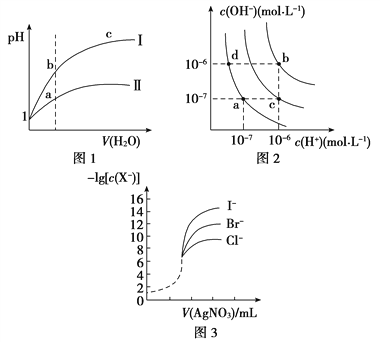
A. 图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B. 图2中纯水仅升高温度,就可以从a点变到c点
C. 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
D. 用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
【答案】C
【解析】试题分析:A.盐酸是强酸,完全电离,醋酸是弱酸,部分电离,当开始时二者的pH相同,溶液中c(H+)相等,随着加水稀释,醋酸的电离平衡正向移动,使稀释过程中醋酸溶液中c(H+)大于盐酸,所以稀释相同倍数时盐酸的pH变化较大,醋酸的pH变化较小,溶液中离子浓度越大,溶液的导电性就越强,因此反应图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为醋酸,且a点溶液的导电性比b点强,错误;B.水的电离过程是吸热过程,升高温度,促进水的电离,水电离产生的c(H+)、c(OH-)都增大,若是纯水仅升高温度,就可以从a点变到b点,而若从a点变为c点,则还要加入强酸,不是仅升高温度实现,错误;C.图2中在b点对应温度下,Kw=1.0×10-12;将pH=2的H2SO4,c(H+)=10-2mol/L与pH=10的NaOH溶液,c(OH-)=10-2mol/L,二者等体积混合后,则溶液中c酸·V酸=c碱·V碱,n(H+)=n(OH-)所以溶液显中性,正确;D.根据图示可知,AgCl的溶解度最大,AgI的溶解度最小,所以用0. 0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,可确定首先沉淀的是I-,错误。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论一定错误的是
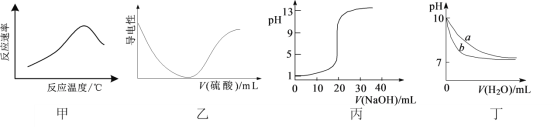
A.图甲表示酶催化反应的反应速率随反应温度的变化
B.图乙表示向BaCl2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化
C.图丙表示用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸的滴定曲线
D.图丁表示相同温度下,向等体积pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化 如图所示。下列叙述中正确的是 ( )
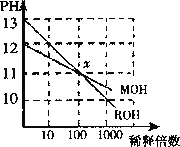
A.ROH是一种强碱
B.在x点,MOH完全电离
C.在x点,c(M+)>c(R+)
D.稀释前,c(ROH)=10c(MOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应的化学方程式中,属于水解反应的是( )
A.H2O+ H2O![]() H3O++OH-
H3O++OH-
B.CO2+H2O![]() H2CO3
H2CO3
C.HCO3-+OH-![]() H2O+CO32-
H2O+CO32-
D.CO32-+ H2O![]() HCO3- +OH-
HCO3- +OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.![]() 含有的电子数为11NA
含有的电子数为11NA
B.![]() 的
的![]() 溶液中氮原子数等于0.6NA
溶液中氮原子数等于0.6NA
C.常温下,![]() 与
与![]() 混合气体中氧原子数为2NA
混合气体中氧原子数为2NA
D.硫酸铵中既含有离子键,又含有共价键,而氯化铵中只含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应: PCl3(g)+Cl2(g)![]() PCl5(g)达平衡时,PCl5为0.40mol,如果此时再移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g)达平衡时,PCl5为0.40mol,如果此时再移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.40molB.0.20mol
C.小于0.20molD.大于0.20mol,小于0.40mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。某实验中将6 mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线 (甲)所示。请完成下列问题:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。某实验中将6 mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线 (甲)所示。请完成下列问题:
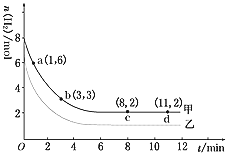
(1)a点正反应速率________逆反应速率(填“>”、“<”或“=”)。
(2)若仅改变某一实验条件再进行一次实验,测得H2的物质的量随时间变化如图中虚线(乙)所示,曲线(乙)对应改变的实验条件可以是________(填序号)。
a.加催化剂 b.增大压强 c.升高温度 d.增大H2浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电源串联电解分别装在两烧杯里的600mL 0.3 mol/L AgNO3 和300 mL 0.5 mol/L的NaCl溶液,以铂作电极,电解一段时间(两烧杯里溶质均有剩余)取出电极,将两杯溶液混合,对混合液的pH判断正确的是 ( )
A.小于7B.大于7C.等于7D.大于或等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如右图所示,下列说法中,正确的是
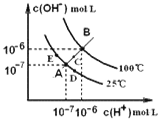
A. 图中A、B、D三点处KW间的关系: B>A>D
B. 100℃,向pH=2的稀硫酸中逐滴加入等体积pH=10的稀氨水,溶液中 c(NH4+)/c(NH3·H2O)减小,充分反应后,溶液到达B点
C. 温度不变,在水中加入适量NH4Cl固体,可从A点变化到C点
D. 加热浓缩A点所示溶液,可从A点变化到B点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com