
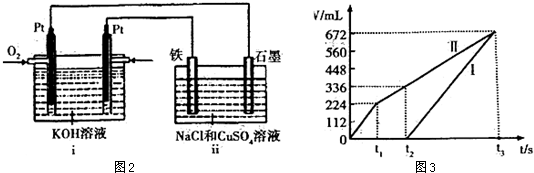
| 0.112×4 |
| 22.4 |
| 0.02mol |
| 0.2L |
| 0.224L |
| 22.4L/mol |
| 0.02mol |
| 0.2L |
| 0.448 |
| 22.4 |
| 0.224 |
| 22.4 |
| 0.1×1 |
| 6 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、①②④⑤ | B、①②④⑥ |
| C、②④⑤ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3 mL 2 mol/L的NaCl溶液 |
| B、50 mL 4 mol/L的FeCl3溶液 |
| C、200 mL 1mol/L的HCl溶液 |
| D、50 mL 3 mol/L的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2+2NaI═2NaCl+I2 | ||||
B、NH4HCO3
| ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、Fe2O3+3CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜没有铁活泼,轮船外壳上可以镶嵌铜块防止腐蚀 |
| B、SO2因为具有强氧化性,可用于漂白草帽 |
| C、氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
| D、明矾水解产生Al(OH)3胶体,可用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
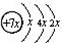 .B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
.B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、物质发生化学变化时一定伴随着吸热现象或放热现象 |
| C、稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D、在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物 |
| C、石炭酸、石油、烧碱分别属于酸、油脂、碱 |
| D、蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com