
【题目】实验室用O2氧化NH3制备硝酸的装置如图所示(夹持装置略),下列说法不正确的是

A.球形干燥管B中可以填充碱石灰或五氧化二磷
B.实验过程中,若熄灭酒精灯,装置C中的氧化铬继续保持红热,说明装置C中的反应放热
C.球形干燥管D中的无水氯化钙可吸收尾气中的氨气和水蒸气
D.装置E中的石蕊试液最终变红,说明锥形瓶中有硝酸产生
科目:高中化学 来源: 题型:
【题目】环氧乙烷(![]() )是一种最简单的环醚,常用于有机合成。某研究小组以环氧乙烷和甲苯为原料按下列流程合成有机化合物G和I。
)是一种最简单的环醚,常用于有机合成。某研究小组以环氧乙烷和甲苯为原料按下列流程合成有机化合物G和I。
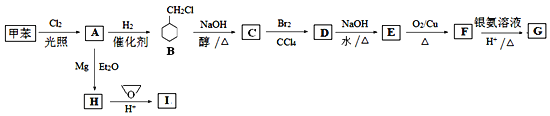
已知:CH3Cl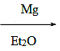 CH3MgCl
CH3MgCl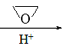 CH3CH2CH2OH
CH3CH2CH2OH
回答下列问题:
(1)A分子中最多有_____个原子共平面。
(2)D的结构简式为_____。
(3)写出下列反应的化学方程式:
E→F:______;G和I在浓硫酸催化下生成酯:______。
(4)I有多种同分异构体,写出其中满足以下条件的同分异构体的结构简式:_______。
①属于芳香族化合物; ② 能与FeCl3溶液发生显色反应;
③核磁共振氢谱显示不同环境的氢原子个数比1:2:3:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH反应生成不同的产物,同学们据此展开探究。
(实验1)甲同学利用如图所示装置进行实验:
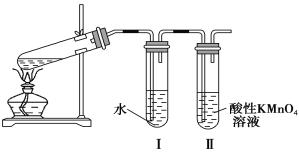
(1)甲同学的实验目的为____________________________。
(2)实验过程中可观察到试管Ⅱ中的现象为__________________________________________________。
(3)试管Ⅰ的作用为_________________________________________________________。
(实验2)乙同学在试管中加入3 mL溴乙烷和3 mL NaOH溶液,振荡,加热。
(4)此反应的化学方程式为_________________________________________。
(5)停止加热并冷却后,欲证明确实发生了上述反应,还应进行的操作为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法不正确的是( )
A. 用报纸包装食物属于资源的充分利用,应以提倡。
B.  是矿泉水瓶、饮料瓶底的常见标志,表示可回收利用,只能一次性使用,不能长期使用。
是矿泉水瓶、饮料瓶底的常见标志,表示可回收利用,只能一次性使用,不能长期使用。
C. 具有吸水性的植物纤维加工后可用作食品干燥剂。
D. 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质互为同分异构体的有
①乙醇和二甲醚 ②正丁烷和异丁烷 ③金刚石和富勒烯 ④![]() 和
和![]() ⑤蔗糖和麦芽糖 ⑥蛋白质和氨基酸
⑤蔗糖和麦芽糖 ⑥蛋白质和氨基酸
A.③④⑥B.①②④C.①②⑤D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕捉、封存与再利用是实现温室气体减排的重要途径之一。
(1)二氧化碳的电子式为___________。
(2)下列利用二氧化碳的反应中原子利用率达100%的是_____(填序号)。
a.CO2+2NH3 ![]() CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4![]() CH3COOH
CH3COOH
c.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
d.
(3)一种正在开发的利用二氧化碳制取甲醇的流程如下:

①反应(Ⅰ)将CO2和H2O转化为甲酸常用途径有两种,如下图(a)和 (b)。

图(a)中能量主要转化方式为____,图(b)中发生反应的化学方程式为_____。
②在5L的恒温恒容密闭容器中充入1moLCO和4molH2,加入催化剂发生反应,测得CO及CH3OH的物质的量随时间变化如下图所示。

图中第______min(填数字)反应达到平衡,CO在0~4min内的平均反应速率比在4~8min内的快,其原因是______;达到平衡时氢气的浓度为______。
(4)已知断裂(或生成)1mol化学键吸收(或放出)的能量称为键能,反应H2(g)+ I2(g)=2HI(g)相关键能数据如下:
化学键 | H—I | H—H | I—I |
键能/kJ·mol-1 | 298.7 | 436.0 | 152.7 |
则该反应的△H为_________kJ·mol-1。
(5)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是_________(不定项选择)。
a.反应速率v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
②某次实验中测得容器内NO及N2的物质的量随时间变化如下图所示,图中v(正)与v(逆)相等的点为______(选填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
物质 | H3PO4 | HF |
电离常数 | Ka1=7.1×103; Ka2=6.3×108; Ka3=4.2×1013 | Ka=6.6×104 |
向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为____________
(2)已知:
Ⅰ.CaO(s)+H2SO4(l)![]() CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
CaSO4(s)+H2O(l) ΔH=-271kJ·mol1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)![]() Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ·mol1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为____________。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率________(填“增大”“减小”或“不变”,下同);HF的平衡浓度________。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH。
CO2(g)+H2(g) ΔH。
①一定温度下,向10L密闭容器中充入0.5mol CO和1mol H2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02mol·L1·min1。则CO的平衡转化率α=________;该反应的平衡常数K=________。
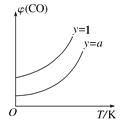
②在压强不变的密闭容器中发生上述反应,设起始的![]() =y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由为_____________
=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a_____1,理由为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对大量盆栽鲜花施用了S﹣诱抗素制剂,以保持鲜花盛开,S﹣诱抗素的分子结构如图,下列关于该分子的说法中正确的是( )
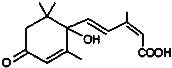
A. 含有碳碳双键、羟基、醛基、羧基
B. 能发生加成反应、氧化反应、取代反应、缩聚反应
C. 1mol该分子能与含2mol NaOH的溶液完全反应
D. 该分子能与溴水反应而使溴水褪色且1mol它能与溴水中的4mol Br2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下, ![]() 。现有1L 0.1mol·L-1的两种溶液:①NaClO溶液;② NaF溶液。下列说法正确的是
。现有1L 0.1mol·L-1的两种溶液:①NaClO溶液;② NaF溶液。下列说法正确的是
A. c(H+):①>②
B. 分别加入1L 0.1mol·L-1HCl溶液后,两溶液的pH:①<②
C. 分别加入等浓度的盐酸至溶液呈中性,消耗盐酸的体积:①<②
D. n(HF)+n(F-)=n(HClO)+n(ClO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com