
【题目】(举一反三)下列说法正确的是( )
A.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解
B.铜与浓硝酸反应的离子方程式为Cu+4H++2NO![]() ===Cu2++2NO2↑+2H2O
===Cu2++2NO2↑+2H2O
C.1.0 mol·L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO![]()
D.硫化铜溶于硝酸的离子方程式为CuS+2H+===H2S↑+Cu2+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是( )
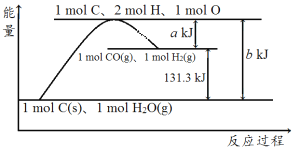
A.反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
B.该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C.amol C和amol H2O(l)反应生成amol CO和a mol H2吸收的热量一定为131.3a kJ
D.1mol C、2mol H、1mol O转变成1mol CO(g)和1mol H2(g)放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在给定条件下离子共存判断及反应的离子方程式均正确的是( )
选项 | 条件 | 离子组 | 离子共存判断及反应的离子方程式 |
A | 滴加氨水 | Na+、Al3+、Cl-、NO3- | 不能大量共存,Al3++3OH-=Al(OH)3↓ |
B | 由水电离出的H+浓度为1×10-12molL-1 |
| 一定能大量共存
|
C | pH=1的溶液 | Fe2+、Al3+、 | 不能大量共存,5Fe2++ |
D | 通入少量SO2气体 | K+、Na+、ClO-、 | 不能大量共存,2ClO-+SO2+H2O=2HClO+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是()
A. 偏二甲肼(C2H8N2)的摩尔质量为60g
B. 6.02×1023个偏二甲肼(C2H8N2)分子的质量为60g
C. 1mol偏二甲肼(C2H8N2)的质量为60g/mol
D. 6g偏二甲肼(C2H8N2)含有NA个偏二甲肼(C2H8N2)分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况会对人体健康造成较大危害的是
A.自来水中通入少量Cl2进行消毒杀菌
B.用SO2漂白食品
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Al2O3样品中含有一定量的Cu、Fe、Fe2O3杂质。现通过下列生产过程,从该样品中提纯Al2O3,并回收铁红。流程如下:
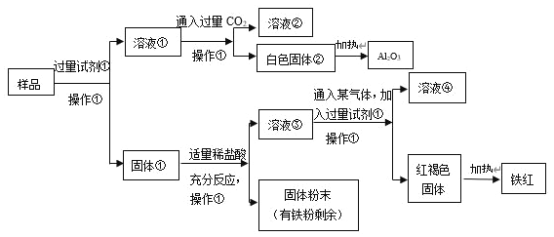
(1)操作①是_________,在实验室进行该操作需要的玻璃仪器有_________。
(2)白色固体②是_________,样品和试剂①反应的化学方程式是_________。
(3)固体①加入适量稀盐酸,可能发生的反应有:_______(用化学方程式表达)。
(4)溶液③中铁元素的存在形式是_________,如何用实验证明:____。
(5)溶液③中通入某气体,该气体可以是_________(任写一种的化学式),红褐色固体制得铁红的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设12C的相对原子质量为24,如果以0.024 kg12C所含的原子数为阿伏加德罗常数,下列数值中肯定不变的是( )
A.氢气的摩尔质量
B.16 g氧气所含的分子数
C.氧气的相对分子质量
D.一定条件下,跟2 g氢气相化合的氧气的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组制备氯气并对产生氯气的条件进行探究。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的___________(填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是___________。
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向_____________。
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是____________________________________________________________。
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。

①已知MnO2呈弱碱性。 Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是___________________________________________________。
②Ⅱ中发生了分解反应,反应的化学方程式是__________________________________。
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:

将实验Ⅲ、Ⅳ作对比,得出的结论是____________________________;
将ⅰ、ⅱ作对比,得出的结论是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com