
【题目】在某密闭容器中,可逆反应:A(g)+B(g)C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
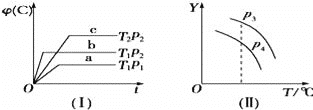
A.p3>p4,Y轴表示A的转化率
B.p3>p4,Y轴表示B的质量分数
C.p3>p4,Y轴表示B的转化率
D.p3>p4,Y轴表示混合气体的平均相对分子质量
【答案】B
【解析】
由图1可知,温度T1时,P2到达平衡的时间短,则反应速率快,所以P2>P1,压强越大,C%越大,则正反应方向为体积减小的方向;压强P2时,T1到达平衡的时间短,则反应速率快,所以T1>T2,温度越高,C%越小,故正反应为放热反应,
A.升高温度平衡向逆反应方向移动,A的转化率减小,增大压强平衡向正反应方向移动,A的转化率增大,则P3>P4,选项A正确;
B.升高温度平衡向逆反应方向移动,B的质量分数增大,增大压强平衡向正反应方向移动,B的质量分数减小,则P3<P4,选项B错误;
C.升高温度平衡向逆反应方向移动,B的转化率减小,增大压强平衡向正反应方向移动,B的转化率增大,则P3>P4,选项C正确;
D.混合气体总质量不变,升高温度平衡向逆反应方向移动,混合气体总物质的量增大,平均相对分子质量减小,增大压强平衡向正反应方向移动,混合气体总物质的量减小,混合气体平均相对分子质量增大,则P3>P4,选项D正确。
答案选B。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】以氨作为燃料的燃料电池,具有能量效率高的特点,另外氨气含氢量高,易液化,方便运输和贮存,是很好的氢源载体。NH3-O2燃料电池的结构如图所示,下列说法正确的是( )
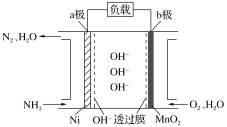
A.a极为电池的正极
B.负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
C.当生成1 mol N2时,电路中通过的电子的物质的量为3 mol
D.外电路的电流方向为从a极流向b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学结合所学知识探究Na2O2与H2能否反应,设计装置如下,下列说法正确的是

A. 装置A气密性的检查方法:直接向长颈漏斗中加水,当漏斗中液面高于试管中液面且高度不变说明气密性良好
B. 装置B中盛放硅胶,目的是除去A中挥发出来的少量水蒸气
C. 装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度
D. 装置A也可直接用于Cu与浓硫酸反应制取SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,完全正确的一组是( )
①用试管夹夹持试管时,将试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过![]() 容积的试管加热
容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,再竖立试管
⑤取用放在细口瓶中液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签对着地面
⑥配制一定物质的量浓度溶液的容量瓶必须先干燥
⑦用坩埚钳夹取加热后的蒸发皿
⑧将胶头滴管垂直伸进试管内滴加液体
⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩检验装置的气密性时,把导管一端浸入水中,用手捂住容器的外壁或用酒精灯微热.
A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑧⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g) ![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是()
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是()
A.A的转化率变大B.平衡向正反应方向移动C.D的质量分数变大 D.a<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I已知下列热化学方程式:
①H2(g)+![]() O2(g)═H2O(l);△H=-285.8kJmol-1
O2(g)═H2O(l);△H=-285.8kJmol-1
②H2(g)+![]() O2(g)═H2O(g);△H=-241.8kJmol-1
O2(g)═H2O(g);△H=-241.8kJmol-1
③CO(g)═C(s)+![]() O2(g);△H=+110.5kJmol-1
O2(g);△H=+110.5kJmol-1
④C(s)+O2(g)═CO2(g);△H=-393.5kJmol-1
回答下列问题:
(1)上述反应中属于放热反应的是_________________
(2)H2的燃烧热△H=___________________
(3)燃烧10gH2生成液态水,放出的热量为________________
(4)表示CO燃烧热的热化学方程式为.________________
II已知:(1)P4(s,白磷)+5O2(g)==P4O10(s)△H1=-2983.2kJ/mol
(2)P(s,红磷)+ ![]() O2(g)=
O2(g)= ![]() P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式_________________。相同的状况下,能量较低的是_________________;白磷的稳定性比红磷_________________(填“高”或“低”)
P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式_________________。相同的状况下,能量较低的是_________________;白磷的稳定性比红磷_________________(填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(s)+B(g) ==3C(g)+4D(g)反应中,表示该反应速率最快的是
A. υ(A)=1.5 mol·L1·s1B. υ(B)=0.5 mol·L1·s1
C. υ(C)=0.8 mol·L1·min1D. υ(D)=4mol·L1·min1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mo1)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
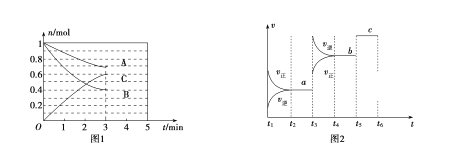
(1)该反应的化学方程式为__________________,此反应平衡常数的表达式为K=________。
(2)从开始到最初达到平衡,C的平均反应速率v(C)=________________。3min时,A的转化率=________%。该反应的![]() ________0。(填“
________0。(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”)
”)
(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡______移动(填“正向”、“逆向”或“不”,下同)
②恒温恒压充入惰性气体,平衡______移动,化学反应速率_______(填“加快”或“减慢”)
③升高温度,平衡______移动。
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是_______,t5时刻改变的外界条件是_______。
②a、b、c三个阶段中,C的体积分数最大的是________,
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3 之间的关系为___________(用“![]() ”、“
”、“![]() ”或“
”或“![]() ”连接)。
”连接)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某有机物和0.5mol氧气在一密闭容器中燃烧得产物为CO2、CO、H2O(气)。产物依次通过浓硫酸时,浓硫酸的质量增加了10.8g;再通过灼热的氧化铜时,氧化铜的质量减轻了3.2g;又通过碱石灰时,碱石灰的质量增加了17.6g。该有机物的化学式为( )
A.C2H4B.C2H6OC.C2H6O2D.C4H6O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com