
����Ŀ��ij���Ӿ��徧���Ľṹ��ͼ��ʾ��X����λ�������嶥�㣬Y����λ�����������ġ���
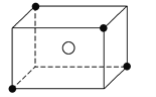
��1��������ÿ��Yͬʱ������__��X��ÿ��Xͬʱ������__��Y���þ���Ļ�ѧʽΪ____________��
��2��������ÿ��X��Χ������ӽ��Ҿ�����ȵ�X����___����
��3�������о��������2��X��1��Y�γɵļнǡ�XYX��____��
��4����þ����Ħ������ΪMg��mol��1�������ܶ�Ϊ��g��cm��3�������ӵ�������ֵΪNA���������������������X���ļ��Ϊ___cm��
���𰸡�4 8 XY2��Y2X 12 109028�� 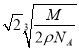
��������
�����Ӿ��徧��ͼ��Xλ��������Ķ��㣬Yλ�����������ģ���1�������к�XΪ4��![]() =
=![]() ����YΪ1��X��Y�����Ӹ���֮��Ϊ1��2��1��Y��4��X�γɿռ���������ṹ�����㾧�����������������ܶȺ�Ħ����������������ı߳����̶�������������������������X���ļ�ľ��룬�Դ������
����YΪ1��X��Y�����Ӹ���֮��Ϊ1��2��1��Y��4��X�γɿռ���������ṹ�����㾧�����������������ܶȺ�Ħ����������������ı߳����̶�������������������������X���ļ�ľ��룬�Դ������
��1�����ݾ����Ľṹ��֪��������ÿ��Yͬʱ������4��X����XΪ���㣬�����γ�8�������壬����ÿ��Xͬʱ������8��Y�������к���1��Y��1/2��X�����Ի�ѧʽΪY2X��XY2������������������ǣ�4��8��XY2��Y2X��
��2��������XΪ���㣬�����γ�8�������壬���Ծ�����ÿ��X��Χ������ӽ��Ҿ�����ȵ�X����3��8��2��12��
�������������������12��
��3����YΪ���ģ�4��Xλ�����������4�������ϣ����Ծ����о��������2��X��1��Y�γɵļн���XYX��109��28����
�������������������109��28�䡣
��4���辧���ı߳�Ϊx������x3��NA/M=1/2�����x��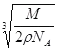 ���������������������X���ľ���Ϊ
���������������������X���ľ���Ϊ![]() x��
x��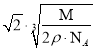 cm��
cm��
����������������ǣ�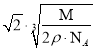 ��
��


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(s)��3B(g)![]() 2C(g)��D(g)��2 min B��Ũ�ȼ���0.6 mol��L��1�������й�˵����ȷ����
2C(g)��D(g)��2 min B��Ũ�ȼ���0.6 mol��L��1�������й�˵����ȷ����
����A��ʾ�ķ�Ӧ������0.4 mol��L��1��min��1
����2 minĩʱ����Ӧ��B�ķ�Ӧ������0.3 mol��L��1��min��1
������2 min����C��ʾ��ƽ������Ϊ0.2 mol��L��1��min��1
����2 minʱ��B��C��D��Ũ�ȱ�һ��Ϊ3��2��1
����D����ʼŨ��Ϊ0.1 mol��L��1����2 minʱD��Ũ��Ϊ0.3 mol��L��1
A. �٢ڢ�B. �ڢ�C. �ܢ�D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ������۲쵽�����ó��Ľ���һ������ȷ����( )
ʵ����� | ���� | ���� | |
A |
| ��ˮ��ɫ |
|
B | �������ữ�� | ��Һ��ɻ�ɫ | �����ԣ� |
C | ����������NaOH���Ҵ���Һ���ȣ������ɵ�����ֱ��ͨ�� |
| ��ϩʹ |
D | ��a��b��֧ʢ�� | a�Թ�����Һ���� b�Թ��в�����ɫ���� |
|
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ɫ��ĩ����BaCl2��K2SO4��CaCO3��NaOH��CuSO4�е�һ�ֻ�����ɣ�Ϊ��̽�����ijɷݣ�����������ʵ�飺�����ж���ȷ���ǣ�������

A. BaCl2��CaCO3һ�����ڣ�NaOH���ܴ���
B. K2SO4��CuSO4һ��������
C. K2SO4��NaOH��CaCO3��BaCl2һ�����ڣ�CuSO4���ܴ���
D. CΪ��һ������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȵĽ�̿��ˮ������Ӧ���ò���ΪH2��CO������CO2��ijУ��ѧ�о�С��������ͼʵ��װ�ü�������е�H2��CO���������������������������й�˵����ȷ����

A. �ڡ��ۡ���������ʢװ����ʯ��ˮ��Ũ���������������Һ
B. Ϊ��ʵ�鰲ȫ����Ӧ�ȵ�ȼ�����ƾ��������ȼ�����ƾ���
C. ����ɫ����ͭ���ɫ������֤��������һ������H2 ��CO
D. ���ü�ʯ���滻��ˮ����ͭ��Ҳ�ɴﵽ����H2 ��COĿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������50mL0.50mol/L���ᡢ50mL0.55mol/LNaOH��Һ����ͼ��ʾװ�ã����вⶨ�к��ȵ�ʵ�飬�õ����е����ݣ�
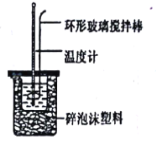
ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
���� | NaOH��Һ | ||
1 | 20.3 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 26.9 |
����������⣺
(1)�����ϱ����������ݣ���ʵ���к��ȡ�H=___�������ؼ���ͻ��������ݼ��ɣ�[�����NaOH��Һ���ܶȰ�1g/cm3���㣬��Ӧ������Һ�ı�����(c)��4.18J/(g����)����]��
(2)�ڸ�ʵ������У���ͬѧ��Ҫ�ⶨ��ʵ��������___������ţ���
A�������Ũ�� B��������¶�
C������������Һ��Ũ�� D������������Һ���¶�
E��ˮ�ı����� F����Ӧ������Һ����ֹ�¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CH4������NO2����Ⱦ����Ӧԭ��Ϊ��CH4(g)+2NO2(g)![]() N2(g) + CO2(g) +2H2O(g)����10L�ܱ������зֱ����0.50mol CH4��1.2molNO2����ò�ͬ�¶���n(CH4)��ʱ��仯���й�ʵ�����������ʾ��
N2(g) + CO2(g) +2H2O(g)����10L�ܱ������зֱ����0.50mol CH4��1.2molNO2����ò�ͬ�¶���n(CH4)��ʱ��仯���й�ʵ�����������ʾ��

����˵����ȷ����
A.������0 ~20 min�ڣ�NO2��������Ϊ0.0125molL��1min��1
B.��ʵ�����ݿ�֪�¶�T1��T2
C.40minʱ��������M��Ӧ������Ϊ0.18
D.�÷�Ӧֻ���ڸ����²����Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ�У�������ȷ���ﷴӦ��ɫ�仯����
A.�����е���Ũ���ᣬ�����ڣ�C12H22O11��H2O![]() 2C6H12O6(������)
2C6H12O6(������)
B.ʪ���KI������ֽ��Cl2������2KI��Cl2��2KCl��I2
C.��ϩͨ��Br2��CCl4��Һ�У��Ⱥ�ɫ��ȥ��CH2��CH2��Br2![]()
![]()
D.ͭ˿�ھƾ��������ձ�ں����̲����Ҵ����ֱ�Ϊ�������Ϻ�ɫ��2Cu��O2![]() 2CuO��CH3CH2OH ��CuO
2CuO��CH3CH2OH ��CuO![]() CH3CHO��Cu��H2O
CH3CHO��Cu��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.��֪2C��s��+2O2��g��=2CO2��g����H=a kJmol-1��2C��s��+O2��g��=2CO��g����H=b kJmol-1����a��b
B.ʯī�ͽ��ʯ��ȫȼ�յĻ�ѧ����ʽ���ɱ�ʾΪ��C+O2![]() CO2��������ͬ�����£�12g��ʯī�ͽ��ʯ���ȼ�շų����������
CO2��������ͬ�����£�12g��ʯī�ͽ��ʯ���ȼ�շų����������
C.һ�������£�0.5 mol N2��1.5 mol H2����ij�ܱ������г�ַ�Ӧ����NH3������19.3 kJ���ݴ�ʵ����ʵ��֪���������£�ÿ����1mol NH3������19.3 kJ
D.4 HCl(g)��O2(g)��2Cl2(g)��2H2O(g)�Ƿ��ȷ�Ӧ��Cl-Cl����O=O���ļ��ֱܷ�243kJmol-1��498kkJmol-1����������H-O���ļ��ܱ�H-Cl���ļ��ܴ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com