
【题目】经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

(1)定性分析:
①如图甲可通过观察_____________________________________,定性比较得出结论。
②有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________,
③若H2O2在二氧化锰催化作用下发生反应,曾检测出有物质MnO3出现,写出整个反应过程的两个化学方程式:___________________________,________________________。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是_________________。
【答案】 反应产生气泡的快慢 控制阴离子相同,排除阴离子的干扰 H2O2 +MnO2= MnO3+H2O 2MnO3= 2MnO2+O2↑ 分液漏斗 收集40 mL气体所需要的时间
【解析】(1)①催化剂的不同会引起反应速率的不同,所以根据反应中产生气泡的快慢来定性分析催化剂的催化效果,故答案是:反应产生气泡的快慢。
②为了是实验具有可比性,应该使溶液中的阴离子也相同,这样才能排出阴离子不同可能组成的干扰。故答案是:控制阴离子相同,排除阴离子的干扰
H2O2在二氧化锰催化作用下发生反应,检测出有物质MnO3出现,二氧化锰作为催化剂,MnO3为中间主物,MnO2先转化为MnO3然后又生成为MnO2。整个反应过程的两个化学方程式:H2O2 +MnO2= MnO3+H2O ; 2MnO3= 2MnO2+O2↑。
(2)从外观分析A是分液漏斗,收集相同的体积,因此需要测量所用时间的长短。故答案为:分液漏斗,收集40mL气体所需要的时间。


科目:高中化学 来源: 题型:
【题目】根据相似相溶规则和实际经验,下列叙述不正确的是 ( )
A. 白磷(P4)易溶于CS2,但难溶于水
B. NaCl易溶于水,难溶于CCl4
C. 碘易溶于苯,微溶于水
D. 卤化氢易溶于水,也易溶于CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)实验室制取乙炔___________________。
(2)2 -氯丙烷的消去反应___________________。
(3)用甲苯制TNT的反应___________________。
(4)l,2-二氯乙烷与NaOH溶液共热___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的过程正确的有 ( )
①蛋白质的变性 ②蛋白质的盐析
③胶体聚沉 ④盐类水解
⑤焰色反应 ⑥氧化还原反应
A.①②③④
B.①③④⑥
C.②③④⑤
D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近又发现了一种新能源——“可燃冰”。它的主要成分是甲烷分子的结晶水合物(CH4·nH2O)。其形成过程是:埋于海底地层深处的大量有机质在缺氧环境中,厌氧型细菌把有机质分解,最后形成石油和天然气,其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。这种“可燃冰”的晶体类型是( )
A. 离子晶体 B. 分子晶体 C. 原子晶体 D. 金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1934年,科学家首次从人尿中分离出具有生长素效应的化学物质——吲哚乙酸,吲哚乙酸的结构如图所示。下列有关吲哚乙酸的说法中正确的是

A.吲哚乙酸与苯丙氨酸互为同分异构体
B.吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应
C.1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2
D.吲哚乙酸苯环上的二氯代物共有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有易溶强电解质的混合溶液10 L,其中可能含K+、Ba2+、Na+、![]() 、Cl、
、Cl、![]() 、
、![]() 、OH中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下图所示:
、OH中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下图所示:
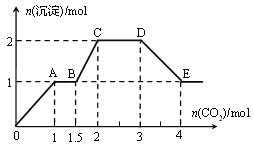
下列说法正确的是
A.该溶液中能确定存在的离子是Ba2+、![]() 、
、![]()
B.肯定不存在的离子是![]() 、OH
、OH
C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2 mol·L1
D.OA 段反应的离子方程式:2![]() +CO2+3H2O===2Al(OH)3↓+
+CO2+3H2O===2Al(OH)3↓+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(含有Cu2O(主要)、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知:Cu2O+2H+=Cu+Cu2++H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是______________.
(2)反应Ⅰ完成后,铁元素的存在形式为_____________.(填离子符号)请写出生成该离子的离子方程式_________________________.
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为_____________。
(4)书写出由沉淀C制备铝的化学方程式:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com