
【题目】下列气体能使湿润的蓝色石蕊试纸最终变红的是 ( )
A.NH3B.SO2C.Cl2D.CO
科目:高中化学 来源: 题型:
【题目】稀土是我国战略性资源.氟碳铈矿主要化学成分为CeFCO3 , 它是提取铈族稀土元素的重要矿物原料.关于氟碳铈矿的冶炼处理工艺已经发展到十数种,其中一种提取铈的工艺流程如下:
请回答下列问题
(1)为增大反应速率,提高原料的利用率,焙烧前可将矿石处理.
(2)焙烧过程中产生的SO3尾气常采用喷淋法净化,再用石灰乳中和;操作I中滤渣的主要成分是 .
(3)操作II若在实验室中进行,需要的主要玻璃仪器有、烧杯、玻璃棒等;所用萃取剂HT需具备的条件是 .
①HT不溶于水,也不和水反应
②Ce3+不和萃取剂HT发生反应
③Ce3+在萃取剂HT中溶解度大于水
④萃取剂HT的密度一定大于水
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:2Ce3+ (水层)+6HT(有机层)2CeT3(有机层)+6H+(水层)从平衡角度解释:向CeT3 (有机层)加入稀硫酸获得较纯的含Ce3+的水溶液的原因是 .
(5)常温下,含Ce3+溶液加碱调至pH=8时,c(Ce3+)=b molL﹣1 , 已知Ce(OH)3的溶度积=a,则a和b的关系是 .
(6)写出Ce(OH)3悬浊液通入氧气得到产品的化学方程式: .
(7)取上述流程中得到的Ce(OH)4产品0.545g,加硫酸溶解后,用0.100 0molL﹣1 FeSO4标准溶液滴定至终点时(铈被还原为Ce3+),消耗25.00mL标准溶液.该产品中Ce(OH)4的质量分数为[Ce(OH)4的相对分子质量为208,结果保留两位有效数字].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)已知H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJmol﹣1 . 若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ.则三者的由小到大关系是(用Q1、Q2、Q3表示).
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是; 若实验中不加盖泡沫塑料板,则求得的中和热数值(填偏大、偏小、无影响) 
(3)实验室用50mL 0.50molL﹣1盐酸、50mL 0.55molL﹣1NaOH溶液利用如图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3 , 又知中和后生成溶液的比热容c=4.18J/(g℃).为了计算中和热,实验时还需测量的数据有(填序号) .
A.反应前盐酸的温度
B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.4 |
2 | 20.2 | 20.4 | 23.6 |
3 | 20.5 | 20.6 | 23.8 |
依据该学生的实验数据计算,该实验测得的中和热△H为 . (保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物说法正确是的
A. 有机物可分烃和烃的衍生物B. 含有碳、氢元素的化合物叫烃
C. 有机物都不溶于水,但易溶于有机溶剂D. 有机物都能燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物X(C7H8O)与另一有机化合物Y发生如下反应生成化合物Z(C11H14O2):![]()
(1)X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是(填字母)。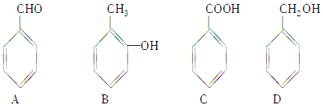
(2)Y的分子式是 , 可能的结构简式是和。
(3)Y有多种同分异构体,其中一种同分异构体E发生银镜反应后,其产物经酸化可得到F(C4H8O3)。F可发生如下反应:![]()
该反应的类型是 , E的结构简式是。
(4)若Y与E具有相同的碳链,则Z的结构简式为?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法正确的是( )
①硅在自然界中以游离态和化合态两种形式存在 ②水泥是硅酸盐材料 ③单质硅是良好的半导体 ④氮化硅陶瓷是新型的无机非金属材料 ⑤光导纤维属于硅酸盐产品 ⑥水玻璃可以用作木材防火剂
A. ①③④⑥ B. ②③④⑤ C. ①②⑤⑥ D. ②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】5.76g部分氧化的Fe、Cu合金样品(氧化产物为Fe2O3、CuO),经如下处理,下列说法正确的是( ) 
A.V=224
B.样品中Fe的质量为2.14 g
C.未氧化前Fe元素的质量分数约为41.2%
D.样品中CuO的质量为3.52 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是人体必需的微量元素,它与脂类代谢有密切联系,但铬过量会引起污染,危害人类健康.
(1)不同价态的铬毒性不同,三价铬对人体几乎无毒,六价铬的毒性约为三价铬的100倍.电镀厂产生的镀铜废水中往往含有一定量的Cr2O72﹣ , 处理该废水常用的流程如图1所示:
Na2S2O3在此过程中表现性.若向含Cr3+的废水中加入过量NaOH溶液,会得到NaCrO2溶液,NaCrO2中Cr元素的化合价为价,反应的离子方程式为 .
(2)交警常用一种“酒精检测仪”检测司机是否酒后驾车.其反应原理如下,请配平该反应方程式:CrO3+CH3CH2OH+H2SO4﹣CH3CHO+Cr2(SO4)3+H2O
(3)已知存在平衡:2CrO42﹣+2H+Cr2O72﹣+H2O.向K2Cr2O7溶液中加入Ba(NO3)2和Pb(NO3)2溶液,可析出BaCrO4和PbCrO4两种沉淀,反应的离子方程式为(任意写出其中一种即可).此时溶液中c(Pb2+):c(Ba2+)= .
已知Ksp(BaCrO4)=1.25×10﹣10;Ksp(PbCrO4)=2.75×10﹣13
(4)工业上以铬酸钾(K2CrO4)为原料,采用电化学法制备K2Cr2O7 , 制备装置如图2所示(阳离子交换膜只允许阳离子透过).通电后阳极的电极反应式为 . 请结合方程式解释反应一段时间后,在阴极室得到浓KOH溶液的原因 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com