

分析 (1)C装置是不需要加热制备氨气的装置,利用浓氨水滴入生石灰产生氨气,与制取干燥氨气可以用碱石灰干燥氨气;
(2)二氧化锰和浓盐酸加热反应制备氯气,浓盐酸易挥发,所以生成的氯气中含有氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
(3)实验时打开开关1、3,关闭2向烧瓶中通入氯气,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的氨气,实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,依据反应化学方程式判断是生成的氯化氢和氨气反应生成的氯化铵;
(4)氯气的氧化性强于溴;
(5)依据实验室制备乙烯的实验装置解答,乙烯制备需要控制反应温度170°C,实验装置中需要用温度计控制反应液的温度;
制取的乙烯中含有二氧化硫,二氧化硫具有还原性,对乙烯与溴水反应造成干扰,应用氢氧化钠溶液吸收.
解答 解:(1)C装置是不需要加热制备氨气的装置,利用浓氨水滴入生石灰产生氨气,制取干燥氨气可以用碱石灰干燥氨气;为制取干燥氨气,可将装置C连接D点的干燥的氨气,装置C中的烧瓶内固体宜选用碱石灰和生石灰;
故答案为:D; a、d;
(2)二氧化锰和浓盐酸加热反应制备氯气,浓盐酸易挥发,所以生成的氯气中含有氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
故答案为:饱和食盐水、浓硫酸;
(3)实验时打开开关1、3,关闭2向烧瓶中通入氯气,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的氨气,实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,依据反应化学方程式判断是生成的氯化氢和氨气反应生成的氯化铵,化学方程式:3NH3+3Cl2=NH4Cl+N2+5HCl;
故答案为:氯气;3NH3+3Cl2=NH4Cl+N2+5HCl;
(4)氯气氧化性强于溴,能够与溴离子发生氧化还原反应置换出溴,溴单质溶液水呈橙红色;
故答案为:装置E中的NaBr溶液变橙红色;
(5)若利用装置A、E进行乙烯与溴水反应的实验,装置A是乙烯制备装置,需要控制反应温度170°C,实验装置中需要用温度计控制反应液的温度,向烧瓶中插入一只温度计,并使温度计水银球没入烧瓶内液面下;
制取的乙烯中含有二氧化硫,二氧化硫具有还原性,对乙烯与溴水反应实验造成干扰,乙烯不溶于水与氢氧化钠溶液不反应,二氧化硫能够与氢氧化钠溶液反应,应选择氢氧化钠溶液除去二氧化硫,故选:A;
故答案为:向烧瓶中插入一只温度计,并使温度计水银球没入烧瓶内液面下;A;
点评 本题考查了氨气、氯气、乙烯气体的制备及性质的检验,熟悉制备原理和物质的性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Cu2+、H+、SO42-、Cl- | B. | Na+、Ba2+、NO3-、CO32- | ||
| C. | Al3+、H+、CO32-、Cl- | D. | Ba2+、OH-、Fe2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 题述反应条件下还原性:CO>Pd | |
| B. | 题述反应中PdCl2被氧化 | |
| C. | 在标况下生成11.2 L CO2时,转移的电子为2 mo1 | |
| D. | 题述反应中CO2为氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K3Cr2Cl7 | B. | K3Cr2Cl5 | C. | K3Cr2Cl9 | D. | K2CrCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.022mol•L-1 | B. | 0.045 mol•L-1 | C. | 0.8 mol•L-1 | D. | 0.1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应4FeS2+11O2=2Fe2O3+8SO2中,每生成1molSO2转移电子数为5.5NA | |
| B. | 标准状况下,11.2LO2参加反应转移的电子数一定为2NA | |
| C. | t℃时,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×10-3NA | |
| D. | 50g46%的乙醇水溶液中,含氢原子总数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解氯化钙溶液:2 Cl-+2H2O═Cl2↑+H2↑+2OH- | |
| B. | 向碳酸氢钙溶液中滴入少量氢氧化钠溶液:Ca2++2 HCO3-+2OH-→CaCO3↓+2H2O+CO32- | |
| C. | 在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| D. | 向偏铝酸钠溶液中加入足量的NaHSO4溶液:AlO2-+H++H2O═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
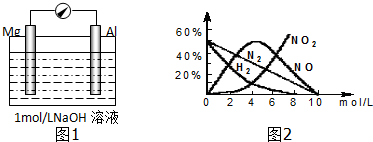
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用饱和食盐水和浓硫酸共热制备HCl气体 | |
| B. | 将H2和Cl2混合,在光照条件下反应,用于工业制备盐酸 | |
| C. | 将Cl2通入饱和石灰水,用于工业生产漂白粉 | |
| D. | 实验室用稀NaOH溶液吸收实验过程中多余的Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com